

| ホームページ | Pirikaで化学 | ブログ | 業務リスト | お問い合わせ |
| Pirikaで化学トップ | 情報化学+教育 | HSP | 化学全般 |
| 情報化学+教育トップ | 情報化学 | MAGICIAN | MOOC | プログラミング |
2012.1.12 (改訂:2014.8.4)
化学、化学工学のプロセスでは、製造工程の合理化は切っても切れません。
造規模を上げて容積効率を上げられればいいのですが、実際には少量多品種の逆に向かっているようです。
そうした時に、例えば今まで10時間時間かかっていた反応が4時間で同じものが作れれば、反応器や熱媒などのエネルギーコスト、人件費などを大幅に削減できます。
こうした反応の加速を考えてみましょう。
日本ゼオンはブタジエン類縁体にDiels-Alder反応で環状付加体を合成し、非常に特徴ある光学レンズ用のモノマーや香料を生産しています。
まず、このDiels-Alder反応をCNDO/2を使って考えてみましょう。
下にブタジエンとエチレンのCNDO/2の計算結果が表示されます。(
これは計算結果を見ているのではありません。与えられた分子の3次元構造に対して、ユーザーのPCでCNDO/2計算した結果を見ている。タブレットでは計算に時間がかかるかもしれません。)
ブタジエンのHOMO、エチレンのLUMOを計算して表示させてみましょう。
水色のキャンバス内でマウスの左ボタンを押したまま動かすと、分子が回転します。
見やすい位置に調整してください。
どちらも、初期にはHOMOの分子軌道図を示しています。
エチレンの方はUpperボタンを押して一つ上の軌道(LUMO)を評させてください。
左に表示されるバーコードのようなものがエネルギー準位を示していて、表示されている分子軌道図のエネルギー順位は赤線で示されています。
いろいろな軌道を確認してください。
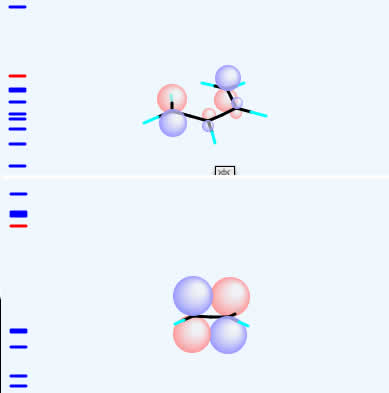
下の左の絵で、2重結合に対して垂直方向に球が上下に表示されています。
これはパイ電子と呼ばれる2重結合を特徴づける分子軌道です。
HOMOとかLUMOの説明はwikiに譲るとして、フロンティア電子論では、分子軌道の位相(左の絵の赤と青の違いは位相が違うという言い方をする)が合う反応が進行するとされる。
この場合、ブタジエンのHOMOとエチレンのLUMOは赤玉と赤玉、青玉と青玉が重なり合って結合になるので環化反応が進むと説明されます。逆にブタジエンのLUMOとエチレンのHOMOでもちゃんと重なります。
しかしエチレンのHOMOとエチレンのLUMOは重ならないので4員環は生成しません。
それでは、工場で大増産させるために、この反応を加速させたいという要望があったら、どのような対応が可能でしょうか?
実際にはケースバイケースでしょうが、例えば下記のケースでは溶媒効果が認められています。
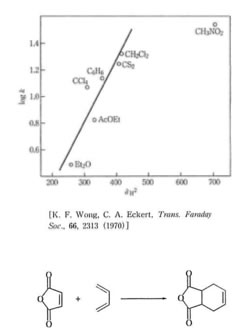
溶媒によって倍以上に反応が加速されています。しかし最も反応を早くする溶媒、ニトロメタンを使いたい(どのような分野に使われているか調べてみましょう)でしょうか? もっと安全で使いやすく、反応が早い溶媒を先手する為に、解析してみましょう。
YMBを用いて、Smilesの構造式から物性推算のテーブルを埋めましょう。
D-A反応溶媒効果データ
課題:
溶媒のどんな物性値が、この反応を加速(log Kが大きい)させているのか特定してみましょう。
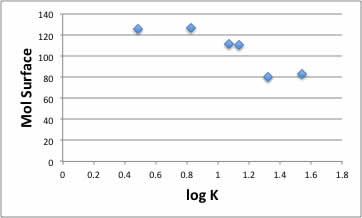
例えば、分子表面積と相関(分子表面積が小さいと反応が早い)があるようにも思えますが、これが本質なのか、たまたまなのか(データ数が増えればすぐに明らかになるでしょうが)化学者としてのセンスが問われます。
他にはどんな物性と相関があるか調べ、論理的に考察してみましょう。
ヒント:Maleic anhydrideの物性も計算してみましょう。
反応を早くする溶媒の大小関係と、反応基質の値を比べてみましょう。
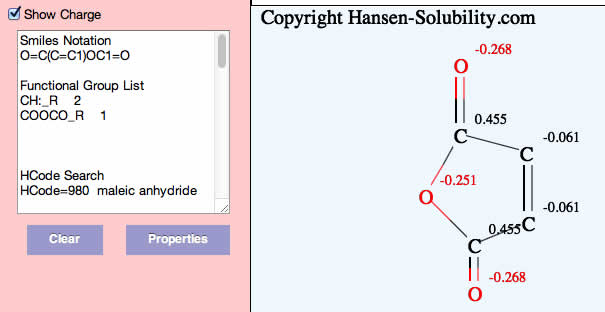
反応溶媒の選定に関しては、非常に多くの場合で、良く溶解するものは高い反応性になります。
その事を念頭入れ、モデル式を構築しましょう。
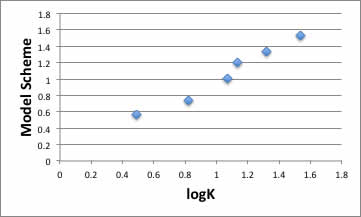
課題:
予測式をたててください。
さらに予測用の溶媒のlog Kを計算しテーブルを埋め、最も反応を加速する溶媒を選定してみましょう。
企業系の研究では、手っ取り早く何点か溶媒を変え合成し、モデル式を立て、さらに効率的な溶媒を探索するのが一般的です。
こうした溶媒を含む計算が分子軌道計算で精度よくできるのはまだまだ先の事と思います。
そうした事を考えると、いまだに、YMBとYSBを使うのが有効だと言えるかも知れません。
これはDiels-Alder反応に限らず様々な反応に応用可能なので、覚えておいてほしいと思います。
産総研のHPでポリ乳酸を作るのにマイクロウエーブ(MW)を使うと反応が加速され、反応時間が1/10になるという記載がありました。
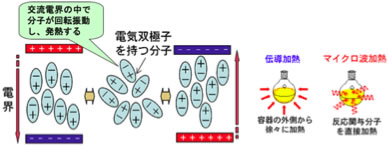
こうした脱水縮合にMWが有効なのはいいのですが、一体どんな反応だったら加速され、どんな反応なら加速されないのか、そのガイディング・プリンシプルが無い事がMWの利用を難しくしていると考えられます。
このMWによる反応の加速をYMBを使って検討してみよう。
ある溶媒に1分間MWを照射した時に温度が何度に達したかのテーブルがあります。(NST、マイクロ波の新しい工業利用技術などから収集しました。)
マイクロウエーブ加熱データ
「いわゆる極性溶媒で無いもの」はMWを照射しても温度は上昇しません。
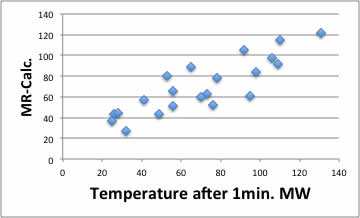
しかし、同じエネルギ-を照射しても、その溶媒が何度に到達したか? は、誘電率やダイポールモーメントだけからでは、下図に示すように判然としません。
(種本では誘電損失と相関があると書いてありますが。。。)
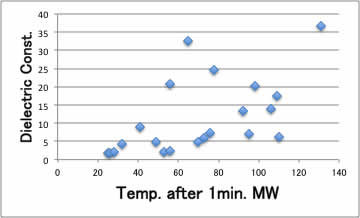
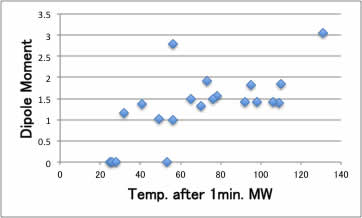
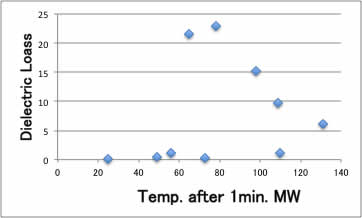
また、実験値の誘電率やダイポールモーメントはあまり多くなく、特に反応基質などのデータはほとんどありません。
そこで、ある基質がMWで分子振動が変わるかどうかを予測する事は難しいのが現状です。
例えば乳酸は室温で固体ですし、こうしたデータが入手できるか考えてみれば意味がわかるでしょう。
課題: YMBで物性推算を行い、どのような物性値と相関があるか確認しましょう。
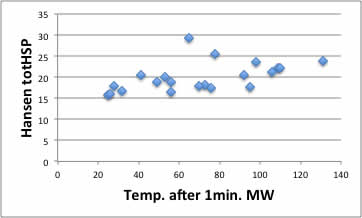
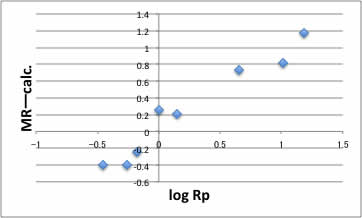
例えばHansen totHSPに対してプロットすると上のグラフのようになります。
溶解度パラメータが大きくなると1分間MWを照射した後の到達温度が高くなる傾向が見られます。
そして2つほど例外がありますが、それらがどうして例外になるのかを考えましょう。
それが説明変数を1つではなく、複数選ぶ時の大事な基準になります。
ハンセンの溶解度パラメータは分子の蒸発エネルギーを
に分割したものです。
totHSPは、その各項をベクトルと見なした時のベクトルの長さになります。
(現在は水素結合項はドナーとアクセプターに分割)
こうした、項目のうちdP項やdH項はマイクロウエーブの感受性に直接関わっていると考えるのは合理的です。
そこで、説明変数を、dD,dP,dHdo,dHacの4つ使うとして、他の物性値としてどんなものを加えるとこの現象をより精度高く推算できるか考えてみましょう。
課題:
HSPの値に加え物性値を2つ選びYSBを用いてモデル式を作成してみましょう。(ヒント:分子の形状に関する情報を付け加える。)その時の乳酸の予測値を求めましょう。
例えば以下のようなグラフが得られ、乳酸の予測値は168℃となり、乳酸は非常に良くMWを吸収し発熱すると予測されます。
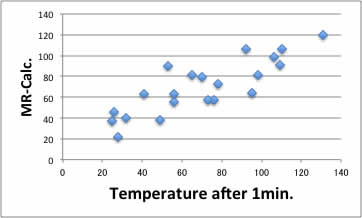
これは実験値で最高のDMFの131℃を大きく上回ります。
そこでポリ乳酸の合成にMWの加速効果が現れるのでしょう。
このパラメータを選択した場合、HSPは温度の関数(蒸発潜熱は温度が高くなると潜熱は小さくなる)ですので、溶媒の温度がMWによって上昇すると加熱効率も下がる事が考えられます。
学生版のYMBでは、25℃以外のHSPは計算できないので、これ以上は精度が上がらないと考える必要があります。
大事な点は、推算式の取り方にはいくらでもバリエーションがあり得るという事です。
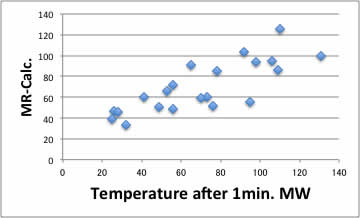
例えば、Antoineの蒸気圧式のA,B,Cと他の物性を組み合わせて推算式を作ってみましょう。
例えば、上図は
到達温度=X*Antoine A+Y*Antoine B+Z*Antoine C +W*MolVolume+V
で計算したものです。
係数を求めてみましょう。
Antoine パラメータは蒸気圧を計算するアントワン式のパラメータです。
それを用いてもまずまずの相関が得られます。
これはAntoine Bというパラメータは蒸発潜熱と相関があり、それはtotHSPと相関があるからです。
またAntoine Cは蒸気圧曲線の曲率を決めるパラメータで、極性化合物ほど値が小さくなるなる事から、こうした物性値をベースにしても予測式は構築する事ができます。
この式でも乳酸の到達温度は159℃となり、HSPをベースとした場合とほぼ一致します。
粘度と熱伝導度を使えば上図のようになります。
到達温度=A*log Viscosity+B*Thermal Conductivity+C*Mol Volume+D
MWの加熱原理に関しては、マイクロウエーブによって分子が回転する事によって摩擦熱によって加熱されるというものがあります。
しかし、それは間違いだと思います。
メラミン樹脂のように、ポリマーであってもマイクロウエーブで加熱されるものがあり、それは回転できません。
到達温度が上図のように粘度と相関がある事から、粘度=分子間の摩擦と単純に理解されたのかもしれません。
私はMWによって分子の安定構造が壊れ、エネルギーの高い分子になり、それが緩和する時に発熱するというエントロピー説が正しいと思っています。
粘度はその緩和に寄与して、熱伝導度は衝突によるエネルギーの授受の効率を表しているので、こうした式でもそこそこ推算ができてしまうと考えています。
乳酸の場合は、255℃とやはり非常に良く加熱されると予測されます。
このように、未知の化合物を予測する時には複数の推算式を構築してその結果を比較検証する事は、非常に重要であると記憶にとどめておいてください。
一般的に考えて、基質がMWで加熱されず、その溶媒がMWで加熱されて、伝導伝熱で基質が加熱されるのであれば、オイルバスなどの熱媒での加熱と同じで、反応時間が1/10になる事は無いと考えられます。
(脱水縮合でできた水がMWで加熱され系外に出やすくなる事はあるかもしれません)
YMBだけで、こうした評価が素早くできるので使わない手はありません。
液体の粘度推算に関してはPirikaのこちらの記事を参照してください 液体の熱伝導度推算に関してはPirikaのこちらの記事を参照してください
鈴木カップリング反応のMWによる加速についてはPirikaのこちらのページを参照してください。
Micro Waveなど、化学工学的に利用されるようになるのはまだまだ先と考えていましたら、氷付けにされたマンモスの解凍にMWが使われたという記事がありました。
普通に解凍すると、内部が溶けるまでに外が腐ってしまうので、MWを使って内部からも解凍し全体を同時に解凍するのが大事なのだそうです。
マンモスを置く部屋一つをMWで均質に加熱できるのなら、化学工学で使うプラントぐらいわけないでしょう。
どういう基質に有効かを見極める、目利きは重要になるに違いありません。
ポリマーをモノマーのタイプ別に分類するなら、今一番多く使われているのはラジカル重合性のモノマーでしょう。
これは過酸化物を加熱する事によってラジカルを発生させて、それがモノマーの2重結合に付加し反応が開始します。
こうした過酸化物は、日本油脂(有機過酸化物国内シェアー55%)、日本パーオキサイドなどが生産しています。ラジカル重合に関してはMOOCのこちらのページを参照してください。
このパーオキサイドの例としてMeOOMeのCNDO/2計算と電荷平衡法計算の結果を見てみましょう。
(CNDO/2についてはPirikaのこちらの記事を参照、電荷平衡法についてはPirikaのこちらのページを参照)してください。
これは計算された結果を見ているのではありません。
CNDO/2の計算と表示プログラムでは、Dimethyl peroxideの構造データがPirikaサーバーから送られてきて、使っているコンピュータ上で実際に計算したものを見ています。
(iPad, iPhoneでは少し計算に時間がかかるかもしれません)
左の部分に青い線があります。
これが分子軌道のエネルギー準位です。
最初に見た時にはそのエネルギー順位はHOMO(Highest Occupied Molecular Orbital)を示してあります(赤い線)。
そのレベルは-14.92eVであることが表示されています。
キャンバス上でマウスをドラッグ(マウスボタンを押したまま左右上下に動かす)してみましょう。
分子が回転して表示されるでしょう。
赤い球と青い球はP軌道を示しています。
回転させるとはっきりわかりますが、この赤と青の球は色が逆転しています。
これは位相が逆で節があるといいます。
つまりパーオキサイドはHOMOが反結合性の軌道であることがわかります。
分子軌道はHOMOまでは電子が詰まっています。
Upperボタンを押してみましょう。
そうするとLUMO(Lowest Unoccupied Molecular Orbital)が表示されます。
LUMOには電子が詰まっておらず、空軌道であるといいいます。
色々なエネルギー準位の分子軌道がどのような形をしているか確認してみましょう。
(注意:この分子軌道の形は速度をあげるため簡略化したものです。単純に半透明の球を描いています。正しくは等高線図で書くので覚えておきましょう。)
このパーオキサイドの結合が反結合性であることが、熱をかけると容易に開裂してラジカルを発生するという特質に繋がっています。
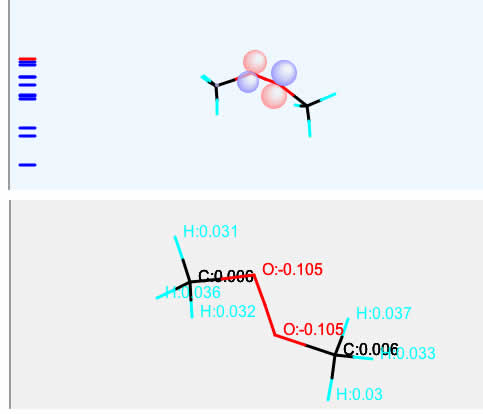
また、電荷をみても酸素が両方とも負電荷なのでその観点からも反発している事は明らかでしょう。
それでは、こうした開裂は溶媒によってどのような影響を受けるのでしょうか?
ポリマーハンドブックにt-butyl peroxideの120℃での分解反応速度が記載されています。
課題:
テーブルの、各溶媒をYMBを使って計算しましょう。 次に、YSBを用いて推算式を構築しましょう。
モデル式=-0.5226*物性1+0.8119*物性2+0.1068*物性3+0.9237*物性4+0.0413*物性5+4.405
どんな物性が分解速度をきめているかを調べ物性を特定し、予測値を計算しましょう。
(ヒント:このページのDiels-Alder反応でも述べたように、溶解性を表す指標が重要です。)
この例で計算してみると、分解反応速度予測値は下図のようになります。
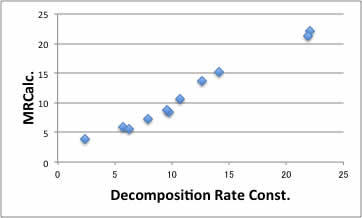
実はこの分解反応は、溶媒の誘電率と相関づけられて説明されています。
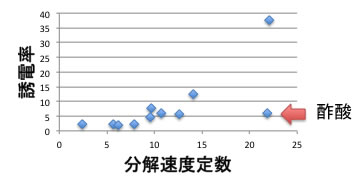
酢酸はダイマーを作るので例外になりますが、誘電率が高くなるほど分解速度定数は大きくなることが教科書に示されています。
しかし実はよくよく見ると同じ誘電率でも(例えば誘電率3で)分解速度定数は大きく異なり、誘電率を見ただけでは(よほど大きいものを除き)分解速度定数を予測する事はできません。
今回作ったモデル式の方がどれだけましか、分かるでしょう。
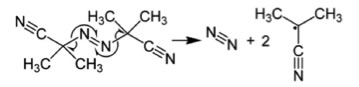
課題: AIBN(アゾビスイソブチロニトリル)の溶媒効果をポリマーハンドブックで調べてみると、下図のようになります。
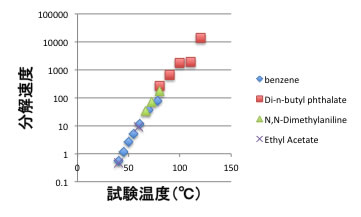
AIBNの分解速度、溶媒依存性データ
溶媒依存性がありません。パーオキサイドとの相違を考察してください。
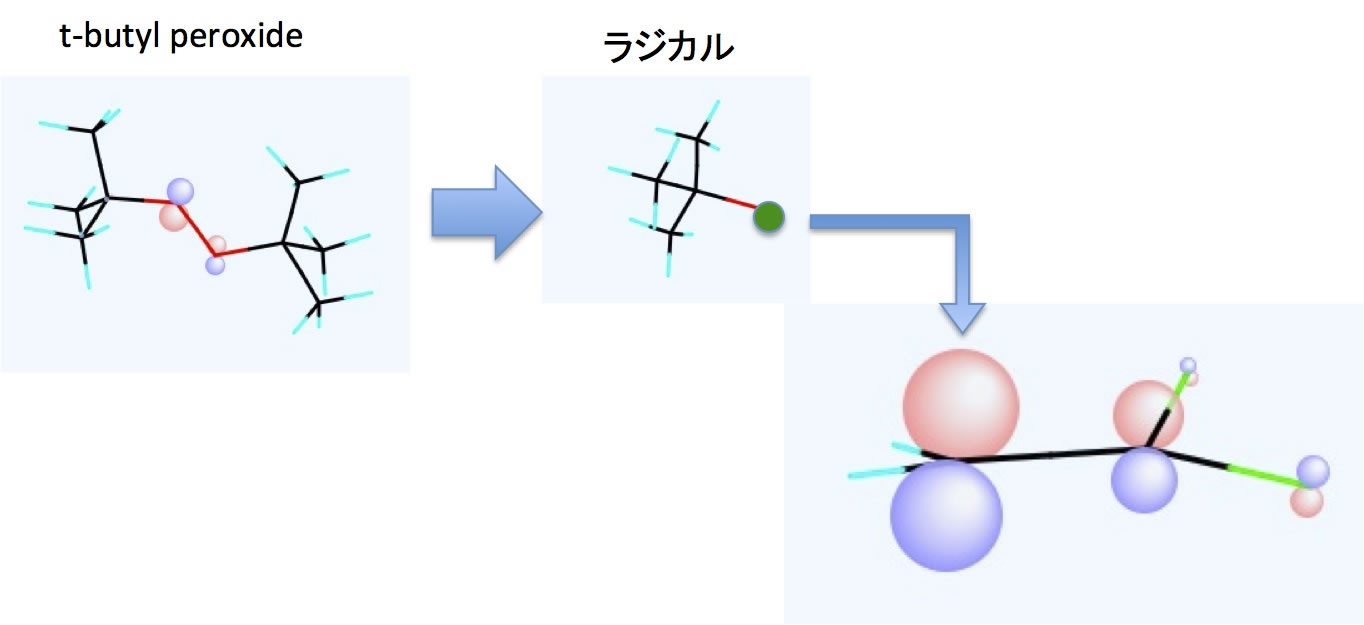
モノマーは2重結合を持知ます。
そこにはC=Cと2重結合に関与する2つの炭素原子があります。
ラジカルはどちらの炭素を攻撃するのでしょうか?
一般的な高分子の教科書では、2重結合に置換基がついた方の炭素を頭(Head)、逆を尾(Tail)と呼び、ラジカルはTailにアタックし、2重結合が消え、Headに新しいラジカルができ、重合が進むと解説されています。
このHead-to-Tailは一般的なラジカル重合性のモノマーで98%程度とされています。
上図のビニリデンフルオライドなどでは、10%以上異結合(Head-Head, Tail-Tail)が含まれるとされています。
では、CF2=CCl2ではどちらがheadでどちらがTailでしょうか?
環状のモノマーではどうでしょうか?
それを知るには上のように分子軌道を計算して軌道の大きさを見なくてはな利ません。
(詳しい事はPirikaのラジカル重合論を参照してください)
そうした用途には、等高線で描かれた分子軌道図よりも上のものの方が見やすい(プログラムを書くのも簡単)ので、自分はこれを採用しています。
この過酸化物は温度が高いほどラジカルは多く発生し、その分ポリマーの重合度は低くなります。
また、溶媒の種類によっても分解速度は大きく異なります。
この溶媒効果も見ておきましょう。
課題:
各溶媒の物性値をYMBを用いて計算しましょう。
次に、モデル式を作成しましょう。 例えば、t-Butyl peroxideの分解反応の時と同じ説明変数を使うと下図のように良好なモデル式が構築できる事が判ります。
この場合でも良好な溶解性は高い反応速度に繋がっている事が示唆されます。
医薬品の合成に使う溶媒が医薬品に残留した場合、最悪体内に投与される可能性があるので、その使用は規制されています。
この残留溶媒に関しては「医薬品の残留溶媒ガイドライン」が,ICH(International Conference on Harmonisation of Technical Requirements for Registration of Pharmaceuticals for Human Use)によって作成されています。
このガイドラインは溶媒を,その毒性によって3つのクラスに分けます。
詳しい事はPirikaのこちらの資料を参照してください。
こうした安全な溶媒を使って反応を行うとして、t-Butyl peroxideや酢酸ビニルの反応を一番早くする溶媒を特定してみましょう。
課題: 次のテーブルの各溶媒の物性値をYMBを使って計算しましょう。
Q3Cのクラス3、4の溶媒データ
次に先に求めたモデル式を使って反応が一番早くなると予測される溶媒を特定しましょう。
このように、YMBの予測値と相関づけるのは何でも良いのです。
収率、選択率などなど。
次にどちらに進んだらいいかの目安を与えてくれます。
うまく使うと様々なプロセスを合理化できます。
Copyright pirika.com since 1999-
Mail: yamahiroXpirika.com (Xを@に置き換えてください) メールの件名は[pirika]で始めてください。