2011.6.24
物性化学トップページ
Pirikaで提供するプログラム
2011-2024年横浜国大(YNU)で行なった授業で使ったYNU-YMBを公開した。
重原子は15まで、CHNO以外の原子は1以下。パラメータは2013年のものなので古い。JSMEの使い方はこちらを参照して欲しい。
以降、2011.6.245の古い記述。
YMBシミュレータ(HTML5 プログラム 2011.6.10)
web版でPass Codeを持たない場合、重原子4つまでしか計算できません。
シス、トランス化合物はその平均値を返します。
芳香族用のパラメター、ハロゲン化合物のパラメーターは入っていません。
(分子の描き方はこちらを参照してください。)
最新の推算方法は、HSPiPに搭載されている。HSPiPに搭載の商用版では、F, Cl, Br, I,S, P, B, Siが使える。芳香族も扱え、最大重原子数は120になる。
プログラムによってどんな原子団が使えるかはこちらで確認のこと
原理
溶解度パラメータ(溶解性パラメータ)にはヒルデブラント(Hildebrand)、ハンセン(Hansen)、Fedors、Van Krevelen、Hoy, Smallなど多くの値がある。
広く流通しているものは、考え方を導き出したHildebrandのものと、それを3次元に拡張したHansenのものであろう。
高分子を扱う研究者は、凝集エネルギー密度からSP値を考える、Fedors、Van Krevelenの方法の方が馴染みがあるかもしれない。
SmallのSP値の推算法はポリマー側に近い。ここでは蒸発潜熱を基本にしたヒルデブラン(Hildebrand)、ハンセン(Hansen)について説明する。
HildebrandのSP値(溶解度パラメータ)は次式で計算される。
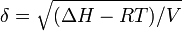
このパラメータはHildebrand とScottによって1964年に提案された(“The Solubility of None-electrolytes.1964)。
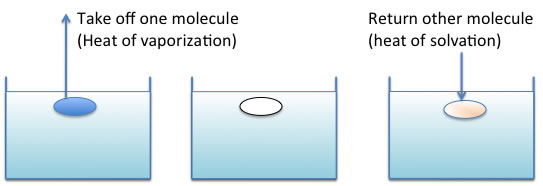
混合の自由エネルギーは次式で書くことができる。
ΔG=ΔH-ΔTS
そして、ΔGが0かマイナスの時に混合は起きる。
ΔH=φ1φ2V(σ1-σ2)2 φ:volume ratio、σ:SP value
ΔHを上のように置いたときに、初めてSP値(σ:溶解度パラメータ)の概念が導入された。
つまり2つの物質のSP値が近いとΔHが0になり、ΔGが0かマイナスになりやすい。
この概念は”似たものは似たものを溶かす”と表現される。
しかし、この方法は自ずと限界がある。似たものと言ったときには、似ているのは構造であってSP値ではないからだ。
例えばエタノールとニトロエタンはほとんど同じSP値を持つが混じり合わない。
これを改良するのに、蒸発のエネルギーを、分散(dD)、分極(dP)、水素結合(dH)の3つに分割したHansenの方法が現在は広く利用されている。
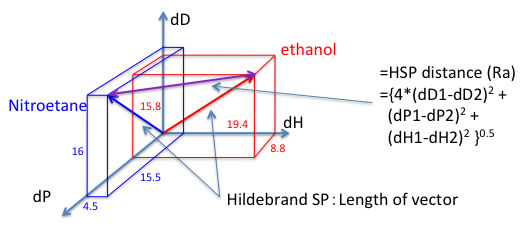
Hildebrandの方法とHansenの方法には次のような関係がある。
Hildebrand SP2 = dD2 + dP2 + dH2
つまりHildebrandの溶解度パラメータは、Hansenの溶解度パラメータのベクトルの長さになる。
従ってHansenの方法は、Hildebrandの方法を完全に包合し、かつベクトルの向きまで含めて”似たもの”を考えることができるのでより優れた方法であると言える。
ハンセンの溶解度パラメータに関する詳しい説明は膨大な資料がPirikaにあるのでそれを参考にしていただきたい。
ここではHildebrandのSP値についてさらに詳しく説明しよう。溶解度パラメータの単位には、(cal/cm3)0.5と(J/cm3)0.5 の2種類がある。昔はcalを使うことが多かったが、最近ではJが一般的である。単純にはcalベースのものを約2倍すれば良い。
このSP値を原子団寄与法を使って推算する方法は多数開発されている。
しかし密度の所でも述べたように原子団基寄与法は原子団の数が増えてくると、値がどんどん大きくなる。
沸点などの物性は値が大きくなっても良いが、密度はそれでは困る。
密度の場合には、分子体積を推算しなくてはならない。それと同様に、SP値の場合には、蒸発潜熱ΔH(分子が大きくなると大きくなる物性)を推算して、
σ={(ΔH-RT)/V}0.5
ΔH:蒸発潜熱、R:ガス定数、V:分子体積(分子が大きくなると大きくなる物性)
の関係を用いて計算しなくてはならない。推算式の形をよく見て利用しないと、とんでもない値を返している事があるので注意が必要である。
YMBシミュレータ(2011年当時の精度)に搭載の方法の精度は以下のようになる。最新の精度はこちらを参照。
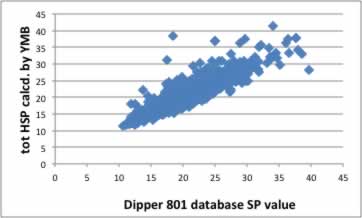
大きく外れるものは、蒸発潜熱自体の推算精度が出ない、カルボキシル化合物である。これらについては分子が大きい物と小さいもので、大きな誤差を持つので、推算値を信じてはならない。
蒸発潜熱の推算
蒸発潜熱の推算法に関してはpirikaのこちらのページにまとめてあるので参照していただきたい。
蒸発潜熱は温度の関数であり、温度の上昇とともに小さくなり、臨界温度に達すると蒸発潜熱はゼロになる。
温度を一定にして熱をかけて蒸発させ、その時の熱量を測定しなくてはならない。
その技術的な困難さから、一番精度が高く蒸発潜熱を測定できるのは沸点の時である。
それは、沸騰の間は温度が変わらないからである。
そこで、HSPの基準になる25℃での蒸発潜熱の値はWatson法を用いて沸点の蒸発潜熱を25℃に変換して用いる。
25℃の分子体積は、分子量を25℃での密度で割れば、分子体積が得られる。
25℃以外の溶解度パラメータ
熱膨張係数をαとした時に
dδD/dT =-1.25*α*δD
dδP/dT =-0.5*α*δP
dδH/dT =-δH (0.00122+0.5*α)
がオフィシャルな計算方法とされている。
しかし、
Thermal Expansion α= a * (1-Tref/Tc)m
式中のaとmは分子に固有の値である。
そこでほとんどの場合は、熱膨張係数をαが求まらないので、HSPiPの中では固定値を使っている。
私は、任意の温度での蒸発潜熱と分子体積を推算する式を構築し、直接、定義式から
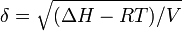
を3成分について計算してしまっている。
ブログを参照して頂きたい。
CED:凝集エネルギー密度からの算出
G(Cohesive Energy:凝集エネルギー)からポリマーのSP値を求める式が数多く開発されている。
σ=(G/V)^0.5
この凝集エネルギーを体積で割った値は、凝集エネルギー密度と呼ばれ、それのルートをとったものが、SP値と定義される。この凝集エネルギーを原子団の数から計算する方法は、Smallの式、Fedorsの式、Hoftyzer-Van krevelen式が知られている。ハンセンの溶解度パラメータを用いて凝集エネルギーを算出するには、
CE=(dD2 +dP2 +dH2 )*Volから算出する。
これをFedorsのものと比較すると、ほとんど完全に一致していることが分かる。
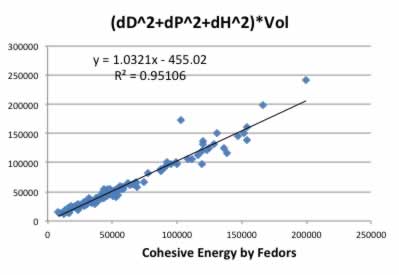
従って、凝集エネルギーを考える場合でも、ハンセンの溶解度パラメータのみを考えれば良い事が分かる。
Hoftyzer-Van krevelenの凝集エネルギーとハンセンの溶解度パラメータから求めたものを比較しても良く一致している。そこでポリマーのトータルの凝集エネルギーが必要なだけなら、ポリマー中にある原子団からハンセンの溶解度パラメータと分子体積を算出すれば良い事が分かる。
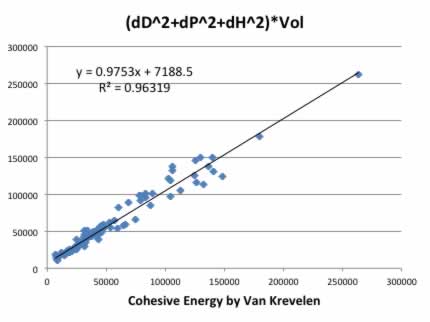
ハンセンの溶解度パラメータで使われる分子体積は、25℃における溶媒の密度と分子量から算出される。
従って液体の分子体積であって、一般に固体のポリマーの分子体積とは異なる。
その関係を求めるためにFedorsの分子体積とHSPの分子体積をプロットし以下の結果を得た。
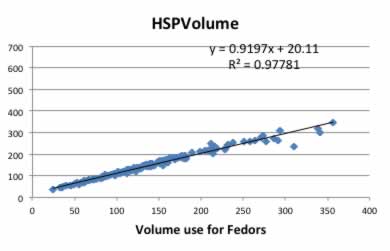
Fedors体積 = (HSP体積-20.11)/0.9197
でポリマーとしての体積を求める事ができる事がわかった。
最新の研究では、ポリマーの繰り返しユニットとポリマーの密度から、ポリマー用の分子体積を推算する式を開発してHSPiPに搭載している。
化合物のSP値は出典によってまちまちの値になり非常に困った状況になる。
物性化学トップページ
Copyright pirika.com since 1999-
Mail: yamahiroXpirika.com (Xを@に置き換えてください)
メールの件名は[pirika]で始めてください。
