2011.4.20
化学工学トップページ >
アントワン定数の算出法
このページの大元となる資料をアップロードした。
分離技術会、講習会2007年 Antoine定数の高度利用
Antoine定数を推算するプログラムは、HSPiPに搭載されました。企業の方はそちらをお使いください。(2013.1.18)
購入方法
Pirikaで提供するフィティング・プログラム
フィティング・プログラムを動かすには、ある温度での蒸気圧のデータが最低3つ以上と沸点のデータが必要です。
HTML5バージョン(2011.4.20)
使い方はこちらを参照
フィティング法まとめ
ExcelやMathematicaを使って、化学の講義をしている大学がある。
それらの中にあるツールは偉大な数学者や統計学者が開発したものだから、ケチのつけようがない。
数学的には正しいのだろう。
しかし、中身もわからずに単純に受け入れてしまうと、化学の分野では困ったことになる。
その例を蒸気圧を計算するAntoine定数のフィティング方法を例に解説しよう。
Antoine定数とは、化合物の蒸気圧と測定温度の間の関係を次の式によって求める為の定数である。
log(P[mmHg])=A-B/(T[℃]+C)
実際にはlog,lnであったり、mmHg,kPaであったり、℃,Kであったりするので、データ集によって値は様々である。
単位系やlog, Ln の違いはさておき、A, B, Cの値がわかれば、任意の温度での蒸気圧が計算できるので非常に便利な式である。
自分は縁があって分離技術会発行の分離ハンドブックの蒸気圧の部分を執筆したので、この分野のデータは非常に多く収集し、自分でアントワン定数を決定しなおすという膨大な作業を行った。
およそ、1900化合物について蒸気圧データから、新たにアントワン定数を決定しなおした。そのような作業をしてみると、例えば化学便覧、改訂4版にある、蟻酸エチル(A=7.0050, B=1130.00, C=217.00)の値が、酢酸メチルのアントワン定数と全く同じことに気がつく。
(自分が作った値と乖離が大きい物をデータベースの値から拾い出してチェックをしていて気がついた。)
蒸気圧のデータは異なっているので、明らかに化学便覧の値が間違っている。
(丸善に問い合せて、間違いを確認した。)
一度出版されると、データは一人歩きをして全てを修正するのは不可能になるので、この問題は非常に本質的な問題だと思う。それはさておき。
このように簡便な方法なのに、最近ではAntoine定数は余り使われなくなってきている。
その理由を説明しよう。
1. Antoine定数は限られた範囲でしか使えない。
例えば、n-octanolの低圧での蒸気圧の測定値で、115℃のデータを±1.5mmHg増減させてAntoine定数を求めてみる。
(蒸気圧のデータは、55℃から115℃、17データポイント)
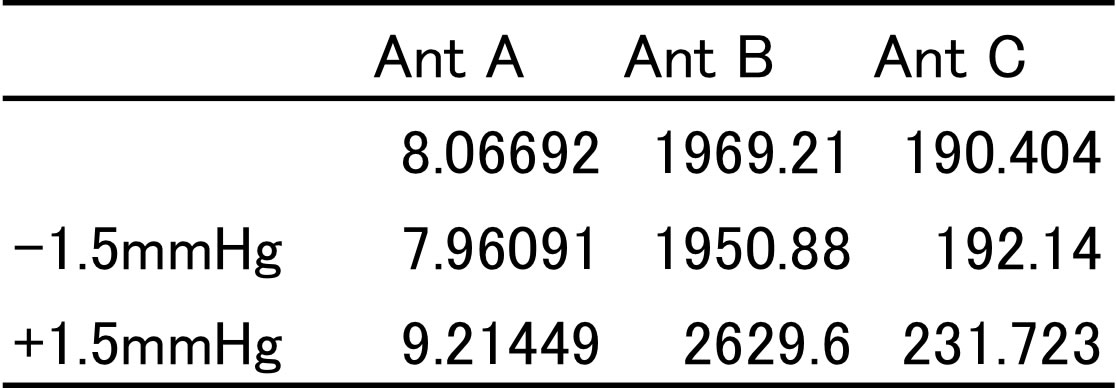
このように測定温度の上限の値を少し変えただけで、アントワン定数は非常に大きく変化してしまう。
そして、このアントワン定数を使って、沸点における蒸気圧を計算すると、その差は260mmHgになってしまう。
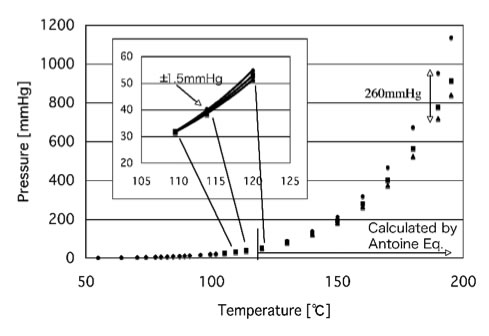
このような事が起きてしまうので、アントワン定数を使う場合には、使える温度範囲を明記して使わなくてはならない。
それでは何故このような事がおきるのだろうか?
その化学的本質を理解せずに、頭から”Antoine定数は限られた範囲でしか使えない”とマニュアル通りに覚えていても無駄である。
これは、アントワン定数を求めるのに、非線形の最小二乗法を使う欠点であり、Antoine法の欠点ではないと自分は考えている。
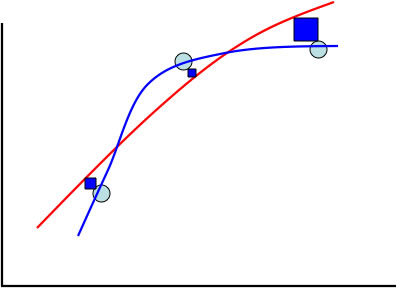
つまり、上の図に示すように、水色の丸の蒸気圧の実験点があったときに、本来ほしい蒸気圧曲線は赤い線だったとしよう。
ところが赤い線と実験点の2乗誤差は青四角に示すように右端で大きな誤差になってしまう。
そこで、アントワン定数を求めるプログラム(多くの場合はマルカート法を用いている)は自乗誤差を最小にしようと、青い線が答えだと言いはる。
論文に書くときなどは誤差が少ないほうが正しくフィッティングできているように錯覚を与えやすいので、こうした値が流通することになる。
2. アントワン法は精度が低いので多定数の蒸気圧式を使うべきである。
- Extended Antoine Equation
log(P[bar])=A-B/(T[K]+C-273.15)+0.43429Xn +EX6 +FX12
( X:(T-to-273.15)/Tc ) - Wagner Equation
ln Pvpr = (aτ + bτ1.5 + cτ3 + dτ6 )/Tr
(τ=1-Tr) - log P = A + B/T + C*logT+DT+ET2
最近では3番目の式が使われる事が多いようである。では、何故このような式を使うのだろうか?
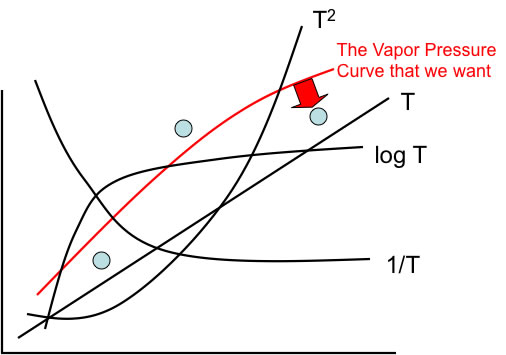
それは、蒸気圧曲線を多数の曲線の和で表すために、例えば端のデータを赤矢印の方向に動かそうとすると、他の曲線の係数が変わり、全体のパーフォマンスが逆に悪くなるためではないかと考えられる。
(それ以上に、Excelを使えば簡単に回帰分析で係数が得られるからかもしれない)
そこで解の安定性が高まるのでこうした蒸気圧式が使われるようになってきているのでは無いかと思う。
ただし、その度合が高まるに連れ、熱力学的な意味合いは薄れていく。
3. アントワン定数は実験誤差に弱い。
自分は実際の蒸気圧の実験データを収集してAntoine定数を決定するときに、このようなデータがあった。
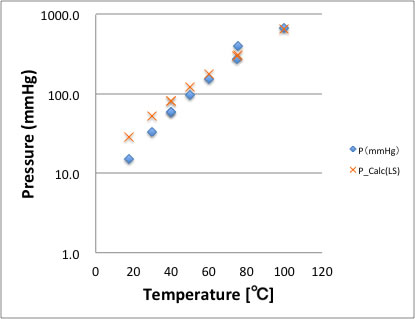
Chloroacetyl chlorideの文献値であるが、明らかに右から2点目のデータは異常値である。
そして、そのデータソースに記載のAntoine定数を使って蒸気圧をプロットすると低温領域で誤差が大きくなる。
このようにマルカート法を使ったフィッティングでは、異常値(実験誤差)があった場合、ひとつの大きな誤差を2乗して評価するため、それに引きずられ、他の部分にも小さな誤差を割り振る。
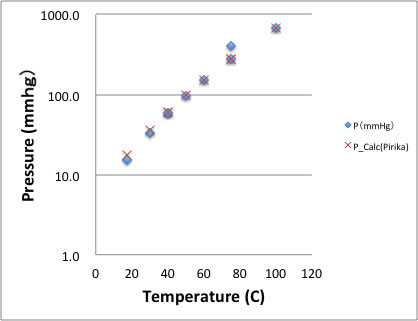
自分が開発した方法では、実験値の異常値(実験誤差)があっても、正しくアントワン定数を決定することができる。
その方法の説明は後述する。
4. 分子の構造のみから定数を決定できない。
これはAntoine式に限るわけでは無いが、フィティングパラメータは分子特有の値であり、構造から推算できないとされてきた。
ところが、自分が開発したAntoine定数決定のプログラムを使って、様々な化合物のAntoine定数を見なおしてみると意外なことが解った。
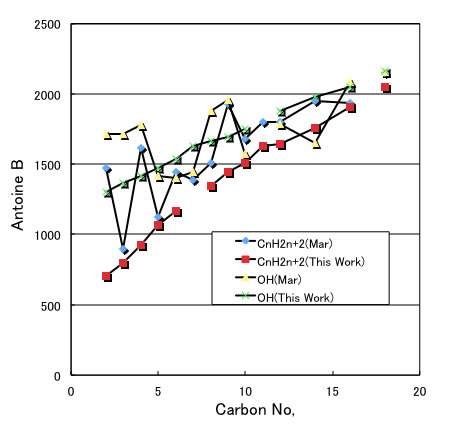
例えばAntoineのBのパラメータだが、マルカート法で決定したものと新しく開発したもので、炭化水素系の化合物とアルコール系の化合物で比較すると上のようなグラフになる。
水色がマルカート法(Mar), 赤色が開発した方法で決めた炭化水素化合物のAntoineのBのパラメータだ。
一見してマルカート法は炭素数が大きくなってもBの値に一貫性が無いことが判る。
それに対して、開発法は分子が大きくなるに連れ、炭化水素化合物でもアルコール化合物でも徐々に値が大きくなることが判る。
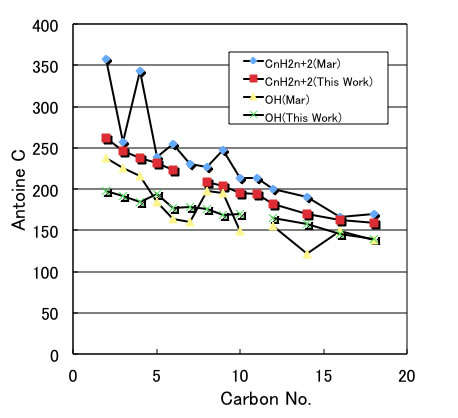
同時にもとまっているAntoineのCのパラメータも同様である。
マルカート法は、A,B,Cの組み合わせで正しく蒸気圧曲線を表現できていれば、分子の大きさなど考慮に入れず答えを出していることが判る。
このようなデータが氾濫しているので、アントワン定数は推算できないという誤解が生まれたのだろう。
自分が決定した1900化合物のAntoine定数は、このように分子構造と強く相関があるため、構造のみから推算することができる。
これを計算する[JAVAのデモアプレット]()があるので、興味が有る方は試してみて頂きたい。
HTML5を使ってiPadでも構造のみから推算できるようにした。
それでは、何故自分が開発したAntoine定数フィティング・プログラムはこのような特徴を持つのだろうか?
それが、化学者の、化学者による、化学者のためのプログラムが必要だという自分の主張につながる。
Antoine定数の本質
まず、蒸気圧というのは熱力学の問題である。そこで、この問題で一番基礎になる式はClausius‐Clapeyron式(1850年)である。
ln(Pvp)=A-B/T B=ΔHv/RΔZv
ΔHv:蒸発潜熱,R:気体定数,ΔZv:圧縮係数の差(狭い範囲でBは温度によらず一定)
例えばエタノールの蒸気圧を温度に対してプロットすると下図のようになる。
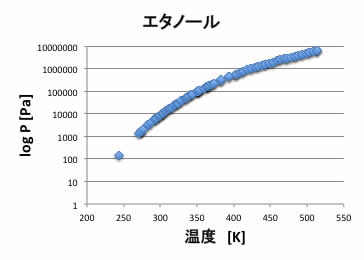
それに対して1000/Tでプロットするとほぼ直線になる。ここでは、B=ΔHv/RΔZv
を1000と置いてしまった訳だが、狭い範囲ではBは温度によらず一定としてよいだろう。
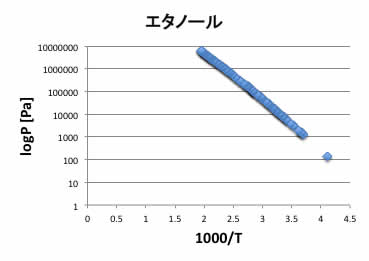
つまり、
Clausius‐Clapeyron式の定数Bは化合物の蒸発潜熱と相関があるはずである。
この式とAntoine式(1888年)log(P[mmHg])=A-B/(T[℃]+C)
を比べてみると、Cの項が無いだけで、同じものであることが判る。
すなわち、Antoine定数のBは蒸発潜熱と相関があるはずである。
そこで、データ集のAntoineのBと蒸発潜熱をプロットしてみた。
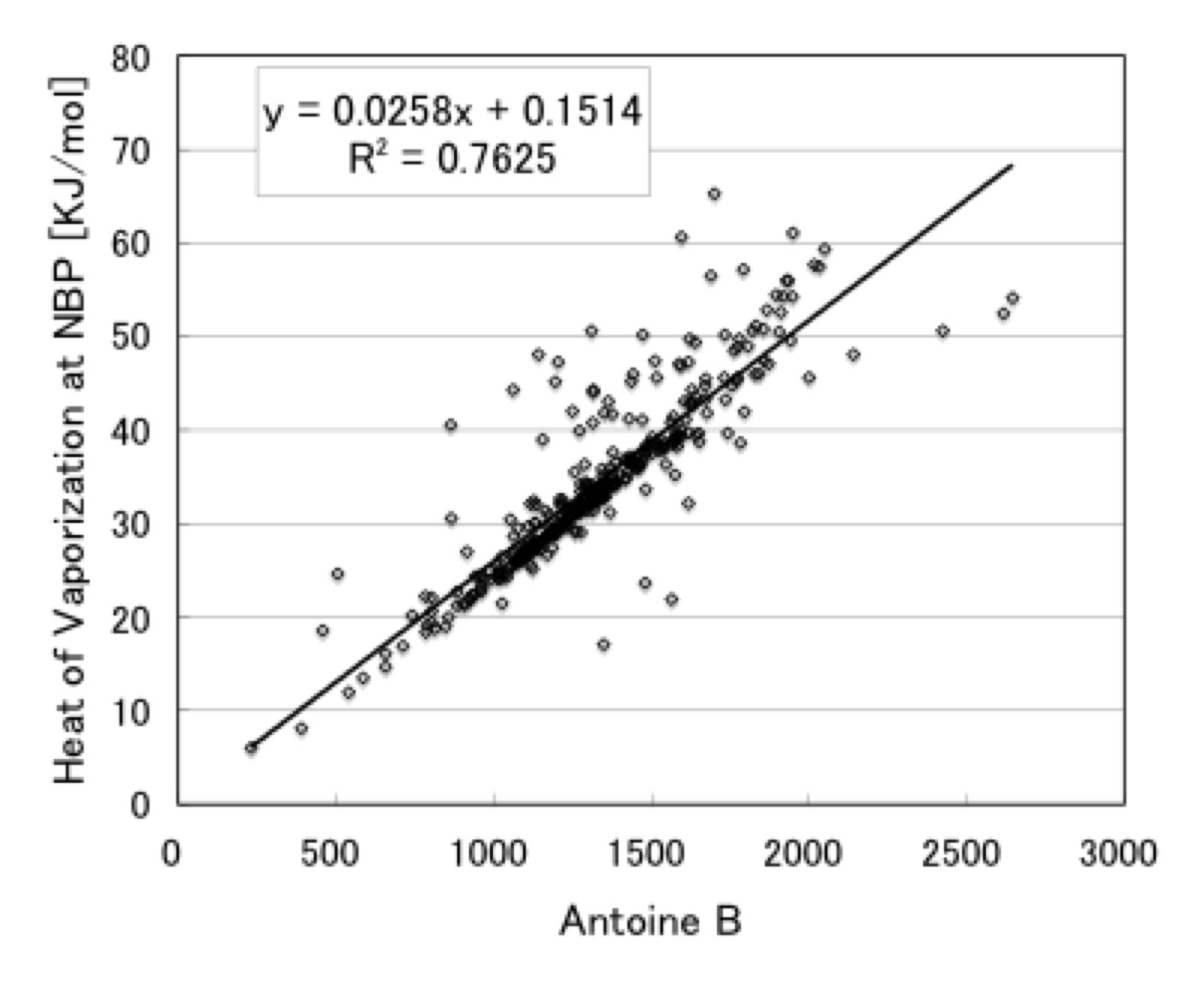
このように、かなり高い相関があるが、一部大きくはずれる化合物により決定係数R2は0.7625と低い値になってしまう。
これはこれまでに説明したようにマルカート法を使ってAntoine定数を決定したことに因る弊害である。
マルカート法は誤差が小さくなるためなら”熱力学など知ったことでは無い” 数学上の答えを返しているに過ぎないことがおわかり頂けると思う。
しかし、一般に化合物の蒸発潜熱を事前に知るのも困難である。
そこでTroutonの通則を使う。
これは沸点と蒸発潜熱の間には、Hv/Tbが大体21ぐらいであるという通則だ。
データー集の値をプロットしてみると以下のようになる。
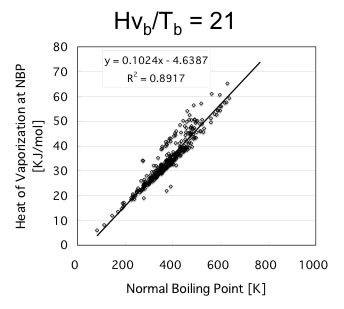
そこで、Antoine Bも沸点と相関が期待できる。
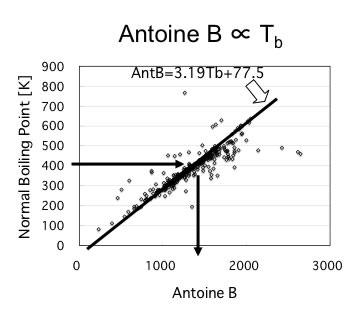
検証してみると上図のようにおおまかに沸点がわかれば、Antoine Bの値の初期値は見当が付けられることがわかる。
それでは、AntoineのCのパラメータは何を意味しているのだろう?
佐藤一雄著
物性定数推算法では、
Antoine C= 240 – 0.20Tb
トンプソン&フィシュティンらの式
Antoine C= -18 + 0.19*Tb
であると記載されている。
実際にデータ集のAntoineのCと沸点をプロットしてみる。
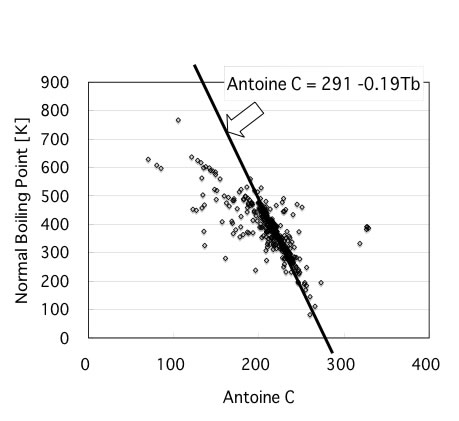
自分が推奨するのは、Antoine C=291 – 0.19Tbだ。
上の2つの式とほとんど同じだ。
これでCの初期値もおおよそ見当がつけられる。
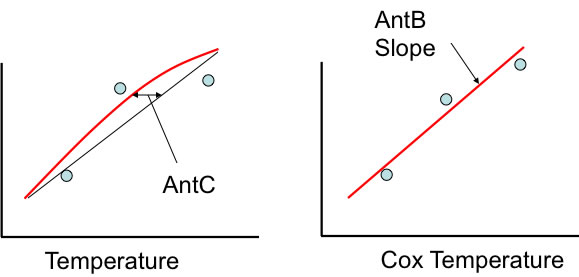
このAntoineB,Cの効果を纏めると、実は1923年に発表されているCox-Antoine線図にたどり着く。
Cox-Antoine線図を簡単に説明すると、
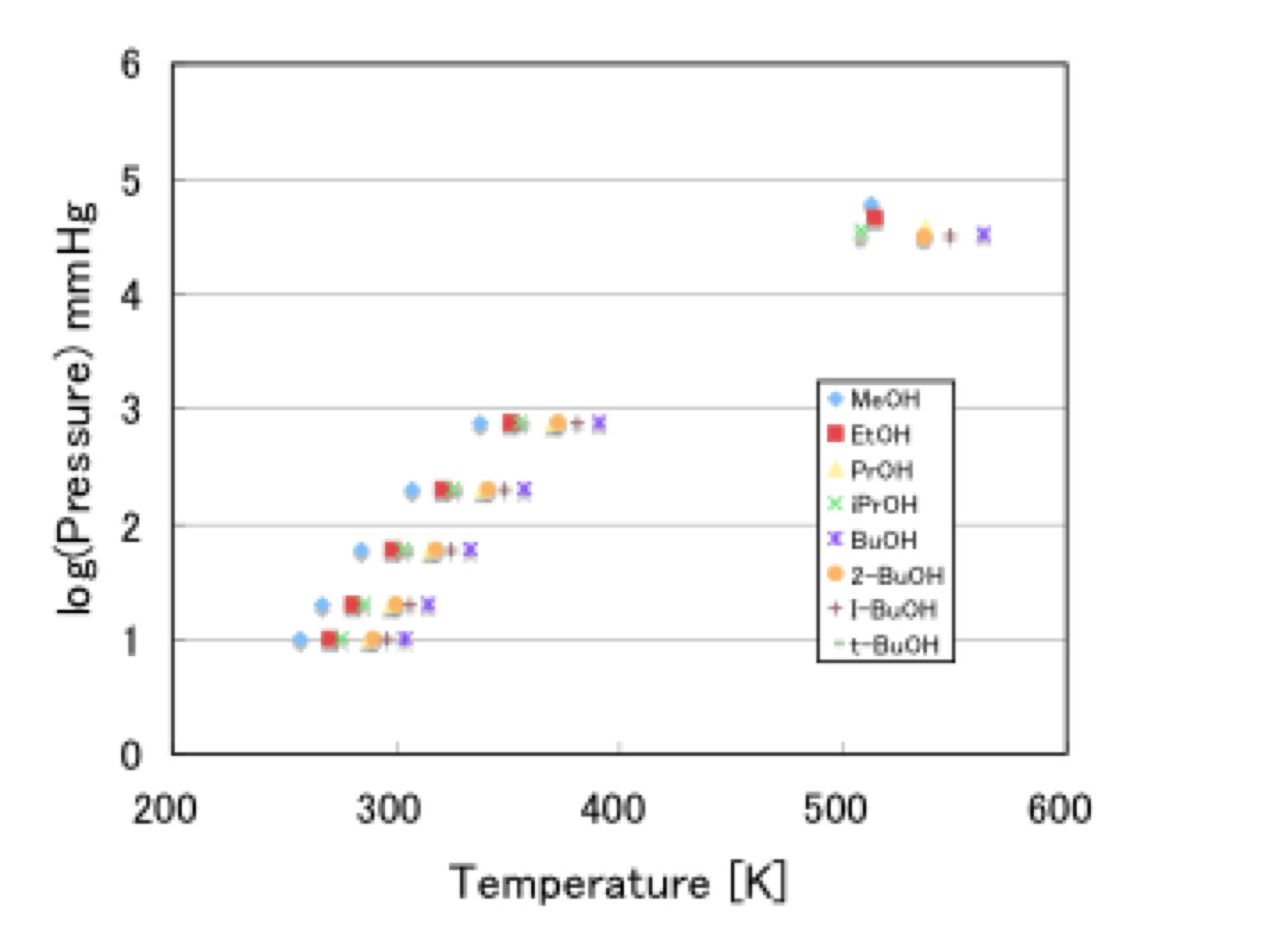
例えば、アルコール化合物の蒸気圧を温度に対してプロットすると上図のような曲線になる。
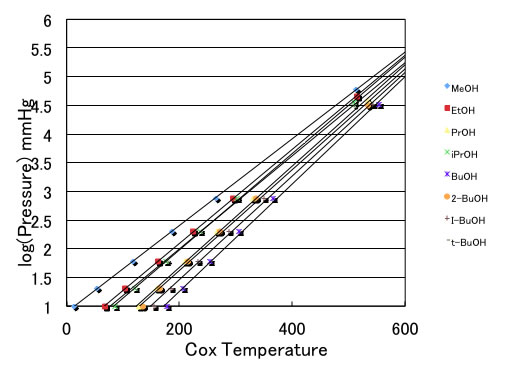
それに対して、横軸をCoxの変換温度に変えると、これらの曲線は直線になる。
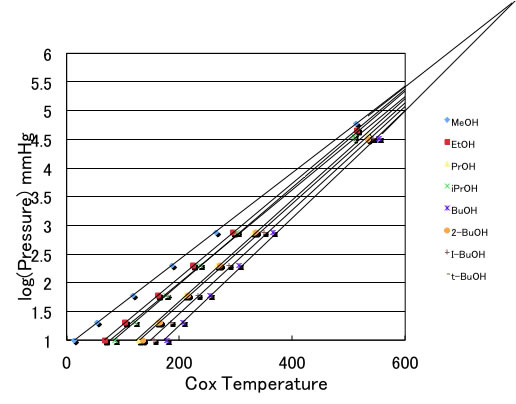
しかも、その直線を延長すると、Cox点と呼ばれる1点で交わる。
Cox点と1点の蒸気圧(沸点760mmHg)があれば蒸気圧曲線を得る事ができる。
沸点以上の高圧部分で精度が高い、という特徴がある。
このCox点は化合物の種類ごとに決まった点になるので、化合物の種類が決まり(Cox点が決まり)沸点がわかれば、蒸気圧直線が得られることになる。
傾きと切片から、近似的には以下の式で計算できる。
log(Pvp)= A- B/(t+230)
化合物の種類によるCox点は
佐藤一雄著
物性定数推算法に一覧があるので参照いただきたい。
(もっといい参考書があったのだが、出てこない。もしご存じの方がおられたら教えて頂きたい。 やっと見つかった。古い資料(昭和38年の本)なので、普通には入手不可能だろう。
散逸しないようにHPに置いておこう。)
このCoxの変換温度の求め方を簡単に説明しよう。
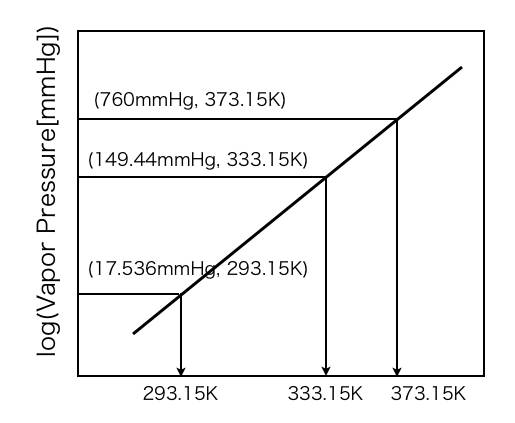
水の293.15K,333.15K,373.15Kの蒸気圧はそれぞれ,17.536mmHg, 149.44mmHg, 760mmHgになる。
この各蒸気圧の対数をとり縦軸におく。
そして適当な斜線を図中に引き,各蒸気圧から横軸に平行な直線を引き,斜線との交点から縦軸に平行な直線を引く。
この直線と横軸の交わった点が温度目盛り(Cox温度目盛り)となる。
この温度目盛りと蒸気圧の対数を用いると,水の蒸気圧曲線は図中の斜線に一致し,完全な直線になる。
こうしてできた圧力と温度の目盛を用いて他の化合物の蒸気圧をプロットすると,その蒸気圧線も直線になるというのが,Cox線図である。
このような便利な方法が廃れてしまったのは非常に残念であるが、線図法は表計算ソフトに乗りにくいし、時代の流れかもしれない。
しかし、基礎は基礎として理解しておく必要がある。
このCox線図とAntoineの蒸気圧曲線の関係を見てみよう。
例としてベンジルアルコールを取り上げる。
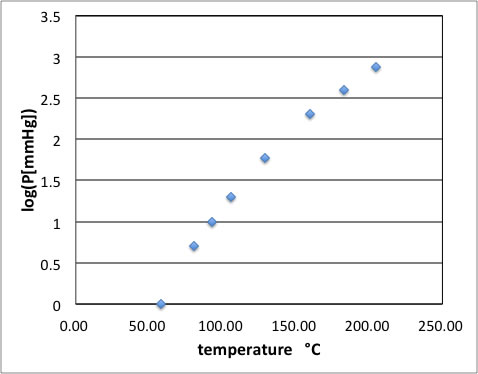
ベンジルアルコールの蒸気圧曲線は上図のようになる。
横軸は通常の温度になる。緩やかにカーブを描いていることがわかる。
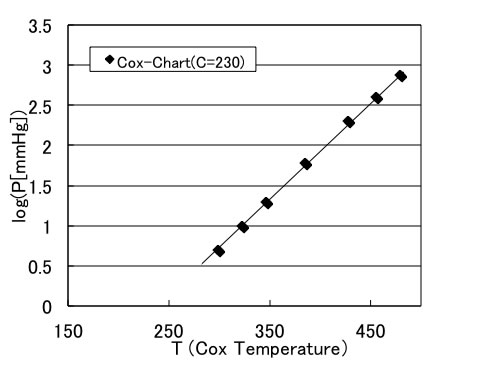
これを温度だけをCox変換温度に変えて、横軸はリニアのままプロットすると、上図のように蒸気圧曲線は直線になる。
(このCox線図を描くソフトウエアーをHTML5+CSS3+JavaScriptで作成した。プログラムは対応するブラウザーでのみ動作します。説明も含めこちらから使ってください。)
同様にAntoineのCのパラメータを178としたときのプロットを行うと、下図のようになる。
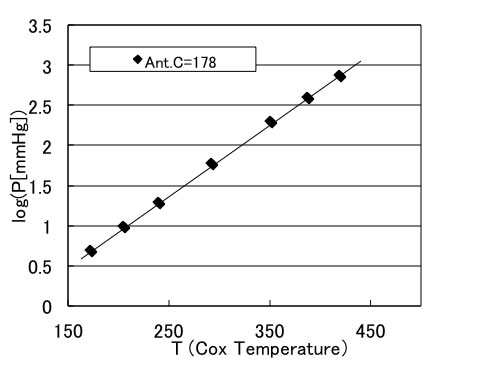
つまり、AntoineのCは曲率の解消の為必要で、AntoineのBは傾きを示し、AntoineのAは切片を示すことがわかる。
このように、熱力学的な意味合いが判ると、構造のみからAntoine定数も推算可能になるだろうと予測もつくし、何故マルカート法ではダメか、どういう蒸気圧フィティング・プログラムを作れば、問題点を解決できるか道筋が見えてくる。
BとCの初期値を最適化する、最小二乗法でないフィティングをするなどの工夫をすれば、熱力学的な意味合いを保持したまま、多変数蒸気圧式よりも解の安定性の優れた蒸気圧式が求まり、その結果を利用すれば分子の構造のみからアントワンパラメータを推算することができる。
こうした、統一的なAntoine定数が得られると物性の温度依存性の理解が飛躍的に高まる。
例えばベンゾニトリル、フルオロベンゼン、エチルベンゼン、ヘキサンの蒸気圧は温度に対して以下のようになる。
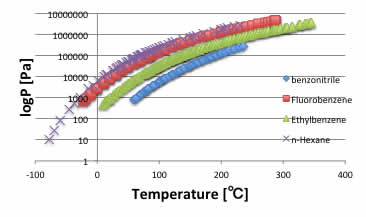
横軸に温度の補正項としてAntoine Cを導入すると、蒸気圧曲線は直線になる。
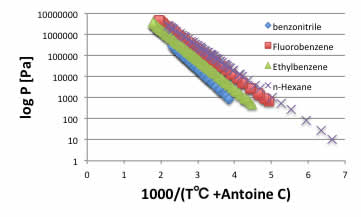
さらにAntoine Bも加えると、蒸気圧曲線はすべて一致する。
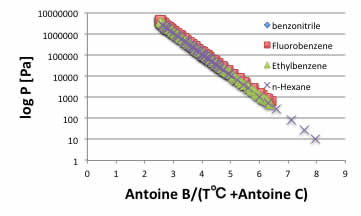
つまり、ある温度を分子に与えた時に、蒸発する分子の量は温度、分子種によって異なるが、Temperatue IndexとしてAntoine B/(T[℃]+Antoine C)で見れば、分子の運動エネルギーは同じになる事を意味している。
その事を利用すると、E-Inkでも説明したようにシリコーンの粘度に対しても、同族体では分子のサイズが異なっても、温度ー粘度の曲線は全て同じになる。
実際に分子構造だけからAntoine定数を計算してみよう。
HTML5+CSS3+JavaScriptのプログラムは対応するブラウザーでのみ動作します。
説明も含めこちらを使ってください。
実験値が一つでもあれば(Antoine のAを実験値から定めれば)精度は非常に高い。
例えば、シックハウス原因物質の25℃での蒸気圧を文献値のAntoine式から求めたものと、沸点のデータがあるものはそれを、無いものは沸点の推算値を使って25℃での蒸気圧を計算した(VP-YMB)を比較すると下のようになる。
| 厚生労働省による濃度指針値のある物質 | BP | VP@25 | VP-YMB |
| アセトアルデヒド | 294 | 899.91 | 890.21 |
| トルエン | 383.78 | 28.40 | 23.90 |
| キシレン | 417.58 | 6.64 | 7.46 |
| エチルベンゼン | 409.35 | 9.48 | 7.81 |
| スチレン | 418.31 | 6.18 | 6.00 |
| パラジクロロベンゼン | 447.21 | 1.79 | 1.45 |
| クロルピリホス | 320F (Decomposes) | 9.2234E-11 | |
| テトラデカン | 526.727 | 0.010046424 | 0.014587166 |
| フタル酸ジ-n-ブチル | 613.15 | 8.40304E-07 | 9.42723E-07 |
| フタル酸ジ-2-エチルヘキシル | 657.15 | 1.94951E-15 | |
| ダイアジノン | 0.000993785 | ||
| フェノブカルブ | 0.000715988 | ||
| 文献値Antoineから | YMB-Antoineから | ||
2012年横浜国大講義資料:塗る太陽電池の設計で、Antoine定数を使った材料設計を紹介した。
基礎物性の推算方法が応用科学にどう使われるか、参照にして頂きたい。
Copyright pirika.com since 1999-
Mail: yamahiroXpirika.com (Xを@に置き換えてください)
メールの件名は[pirika]で始めてください。
