投稿する側に金銭的負担が増えるなど指摘もされているが、私としてはとてもありがたい。引退すると論文が取れないのが一番痛い。
1999年にpirika.comを始めたときには、英語のページのみを公開していた。
Java&Chemistryで「ブラウザー上で化学」を売り物にしていた。
英語にしていたのは、当時は会社員で、工学的な内容をHPに載せた場合に、企業情報漏洩とか言われたく無かったからだ。
日本語のページでは誰が見ても当たり障りないように書いて、裏の英語ページを頑張ったと言うわけだ。
当時は、翻訳ソフトなどないから、英語のページまで調べる酔狂な奴は余りいなかった。
それは、2010年に大学の非常勤講師を始めるまで続き、その後は授業補足資料の公開という形で日本語ページを作り始めた。
大学で教える際に、公開情報以外の事を居住者でない(日本に住んで6ヶ月以上)留学生に教えた場合に「海外輸出管理規定」に抵触する恐れがあると会社が騒ぎ始めたためだ。
授業を取る学生に非居住者がいない事を私に保証しろという。
そこで、授業内容をpirika.comで全部公開すれば、公開情報以外を使った授業は無くなる。ちょうどハンセン先生と仕事を始めた時期だったので、その内容も日本語で公開できるようになったので、私にすれば、「海外輸出管理規定」様さまだ。
pirikaのページは先に論文化してから公開するべきだと、博士を取った(2007年)時の恩師からはよく言われた。
中身的には論文化できるだろうと思う。
でも、企業研究者が、仕事とは別の内容を個人で論文出し続けるというのは不可能だ。金銭的にも時間的にも。
ブログは昨日書いたもので300本になった。pirikaの固定ページを合わせると1000本ぐらいにはなると思う。
これを、20年間、オープン・アクセスの情報として無償で提供してきた。まー、査読は無いけど、研究のオリジナリティーは全世界に知れ渡っている。
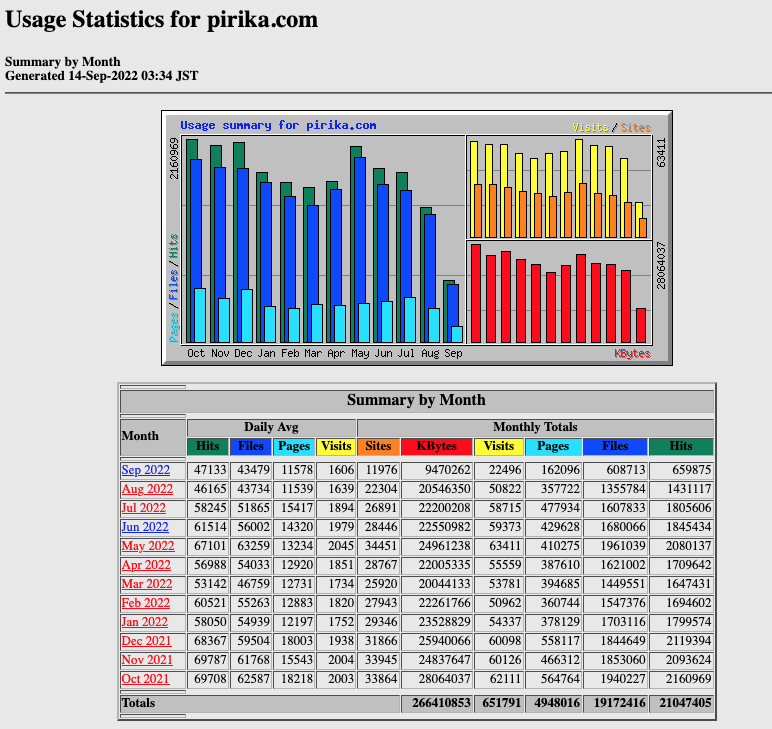
その結果、pirika.comへは、1日あたり1.1〜1.8万ページのアクセスがある。
実際に計算できるページも多いのでリピーターも多いのだろうけど、個人が運営するページとしてはそれなりに誇れる数字だろう(ニッチな化学だけだけど)
一人10円投げ銭してくれれば、もう働かなくていいのだけどなー
現在なら、ブログなどを公開するのはもっとずっと簡単だ。
費用も全くかからないだろう。
レンタルサーバーを借りて、サーバー管理を学んでなんて必要ない。
まー、それにしてもコンスタントに一日1万ページ読まれるようになるのは大変だろうけど。(pirikaに1000ページあれば、平均で10ページしか読まれていない。母数が大事なだけだ。)
OAジャーナル義務化になると、母体の経済状態で、研究者間の格差が広がるとかも言われている。
心配はわかるけど、それより、誰かが読んでくれるような(探してくれるような)ネタを提供できるかだ。
何かを書いて誰かに読んでほしい。その承認欲を満たすことが目的なら、自分の形は有効だと思っている。
論文投稿がインパクトファクターを稼ぎたいのが目的なら話は別だが。
学生にも言っているが、自分で書いたものを世に問いたい(化学系に限るけど)なら、pirika.comにページを作ってあげる。
ゼロベースで始めたって埋もれるだけだ。
タイトルの付け方、見せ方、いろいろ実験すれば良い。
コンテンツ・クリエーターになる一歩だ。
