2024.12.31
情報化学+教育 > YMB Pro for MI >
pirika.comで化学 > 化学全般 > 高分子化学 >
注意:HSPiPに搭載の機能ではありません
経産省の方針で、「自動車メーカーには30年代早期に、乗用車の新車販売でバイオ燃料20%混ぜた燃料への対応車の比率を100%とすることを求める」とありました。YMB24Pro4MIを使って、特にゴムの耐溶剤性(ガソリンとバイオ燃料混合物)を考えてみましょう。
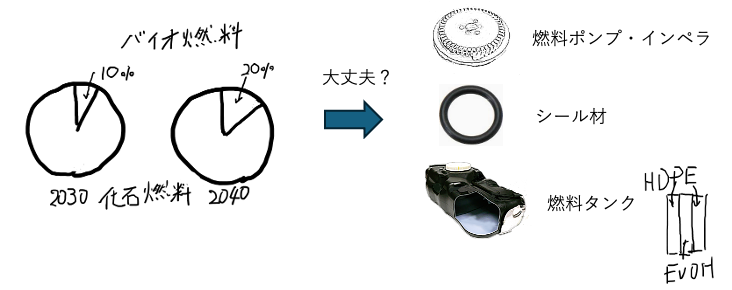
車には様々な高分子が使われています。全てEVにシフトすれば、燃料との適合性は考慮しなくて良くなります。それにしても、ブレーキオイルなどはどうしても使わなくてはなりません。特に日本は原発の電気が利用しにくい事もあって、もうしばらくは化石燃料とのハイブリッド的な利用になると考えられます。その際に化石燃料にバイオ燃料を混ぜて「環境に配慮してます感を出さないといかん」と経産省が考えたのでしょう。日本でそんな混合燃料が供給できるかはともかく、やれ、と言っていれば良いので政治家は気楽なものです。でも、EVが失速して世界中でハイブリッド車が売れている状況を見ると、材料の適合性を見ておくのも悪くはないでしょう。

そもそも、バイオ燃料と簡単に言っても色々な種類があります。最近は天ぷら油の廃油が飛行機用の燃料として取り合いになっているとか。そうしたものとガソリンの混合燃料がゴムを駄目にするかを、事前に予測する技術の開発が望まれています。
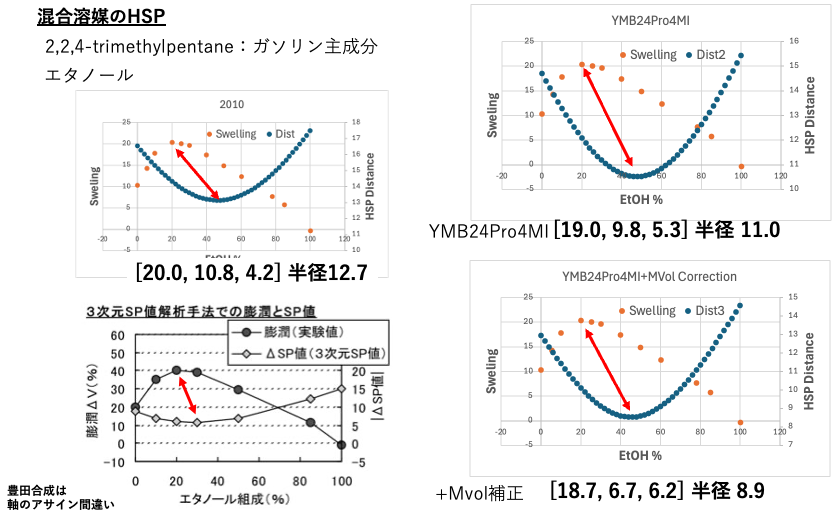
実は2008年に、豊田合成という会社から「3次元SP値による膨潤極値解析技術」という論文が出ています。エタノール自体はNBR(ニトリル・ブタジエン・ゴム)を膨潤させません。ガソリンの主成分のイソオクタンは20%ぐらいNBRを膨潤させます。ところが、イソオクタンにエタノールを20%混ぜるとNBRを40%も膨潤させてしまいます。
ブラジルではガソリンにエタノールが22%混合されています。この燃料に耐えるゴムを作らないとなりません。
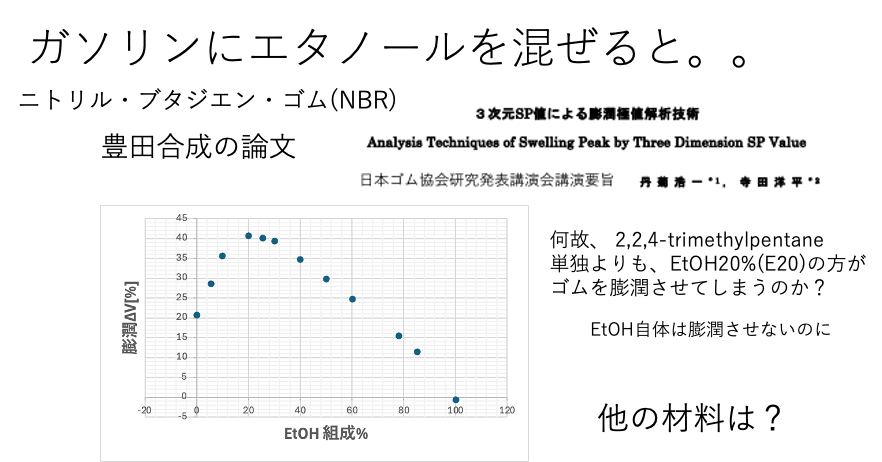
豊田合成の研究者は、混合燃料の膨潤性が上に凸になる非線形性をハンセンの溶解度パラメータ(HSP)で解析しています。私がハンセン先生たちの研究に加わったのが2008年ですから豊田合成はずいぶん早くからHSPを利用していたことになります。
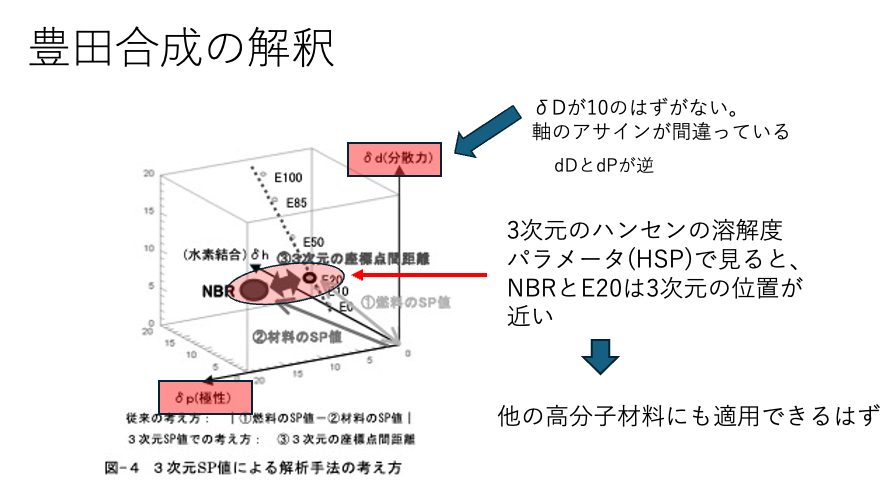
軸のアサインが間違っていますが、彼らは、NBRのHSPとガソリン+20%EtOH混合溶媒のHSPが、3次元のハンセン空間で見ると一番近いと言いたいようです。
この考え方が正しいのなら(もちろん私はHSPの開発者の一員なので正しいと信じていますが)他の材料へも適用できるはずです。
豊田合成の論文中ではNBRのHSP値は記載されていません。軸のアサインが間違っていますが、大体[dD, dP, dH]=[20, 10, 5]ぐらいでしょうか。
それでは、まず、高分子材料のHSPの決定法から始めます。
Hansen先生は、1967年にHSPを発表したときから、Sphere法というやり方を使って高分子材料のHSPを決定していました。

溶媒のHSPは既に決定されています。溶媒のHSP[dD, dP, dH]をベクトルとみなすと各溶媒は3次元座標にプロットすることができます。ただし、ワケがあって座標軸がdDだけ2倍に拡張されています。この空間をハンセン空間と呼びます。そしてその溶媒がポリマーを溶かしたら青く塗ります。溶かさなかったら赤く塗ります。溶かす溶かさないの尺度は研究者が主観で決めます。架橋したゴムの場合、完全には溶け無いので膨潤度できめます。
すると青い溶媒はハンセン空間に集まっていて球(緑色のメッシュ)を形成します。この球をハンセンの溶解球と呼びます。境界のあたりでは入り乱れてしまうことがあります。Sphere法の基礎は、良溶媒がハンセン球の内側に入って、貧溶媒が溶解球の外側に来るハンセンの溶解球を求めることです。その時に誤認識が少なく、最小の半径となる球の中心を探索するのがSphere法です。
このやり方については、「ニトリル・ブタジエンゴム(NBR)の膨潤性とハンセン溶解度パラメータ(HSP)」私のHPに記載しています。
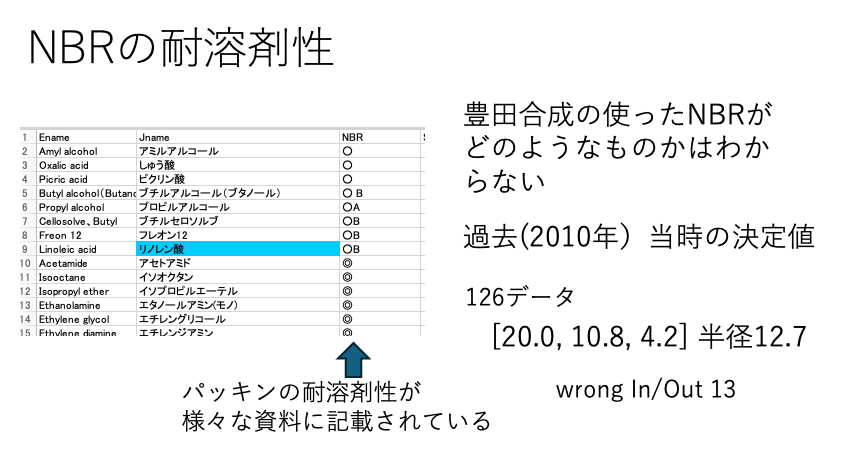
これは、15年も前の話なので、最先端のYMB24Pro4MIを使って解析し直してみます。
HSPiPには、現在の所、次の2式が搭載されています。
1: sqrt(4.0*(dD1-dD2)2+(dP1-dP2)2+(dH1-dH2)2)
3: sqrt( 4.0*(dD1-dD2)2+(dP1-dP2)2+(dHacid1-dHacid2)2+(dHbase1-dHbase2)2)
水素結合項(dH)をdHacid, dHbaseに分割するのは、2010年には確立され、HSPiP ver 3.1から搭載されました。その式は私が作りました。
YMB24Pro4MIでは、このHSPの距離の式を33タイプに拡張しました。HSP距離の33式の詳細に関してはこちらを参照して欲しい。
どの式が一番性能が良いか事前にわかると嬉しいのですが、ケースバイケースで最適な式はことなります。逆に「この式が精度が高かったのは、こういう理由」と理由探しに使います。とても洞察に満ちた答えを出してくれます。
33タイプの式を検討するには、新しい(New Sphere)フォーマットの入力データを準備する必要があります。HSPiPでは入力データを作るのは結構めんどくさいですが、New SphereはCAS番号とScoreだけをExcelに準備します。
データの作成法、距離の式の求め方を説明
書いて説明するのは難しいのでV-tubeを作った。
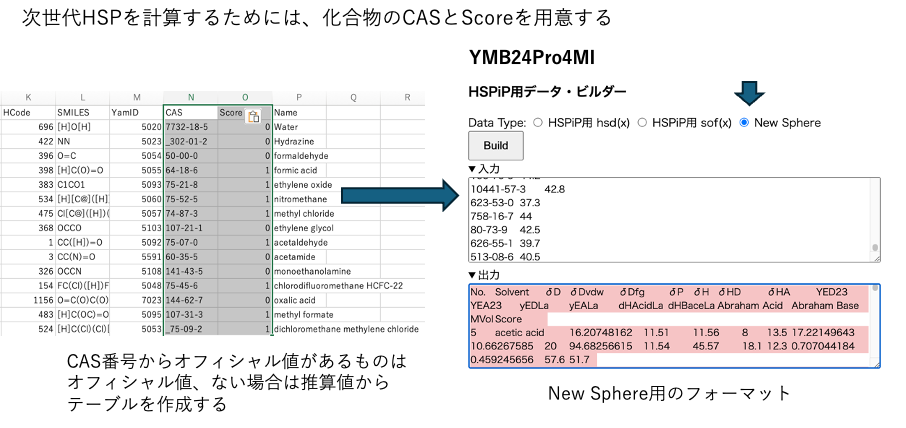
タイトル行も含めて2列をコピーし、HSPiP用データ・ビルダーの入力用の所にペーストし、New Sphereを選んでビルドすれば、出力にNew Sphereデータが作成されます。その際に、CAS番号からDBを検索しオフィシャル値があればオフィシャル値を、無ければ、YMB24Proの推算値でデータセットをつくります。(CASのDBに無い化合物はブランクになります。その時にはSmilesの構造式からデータセットを作ります)
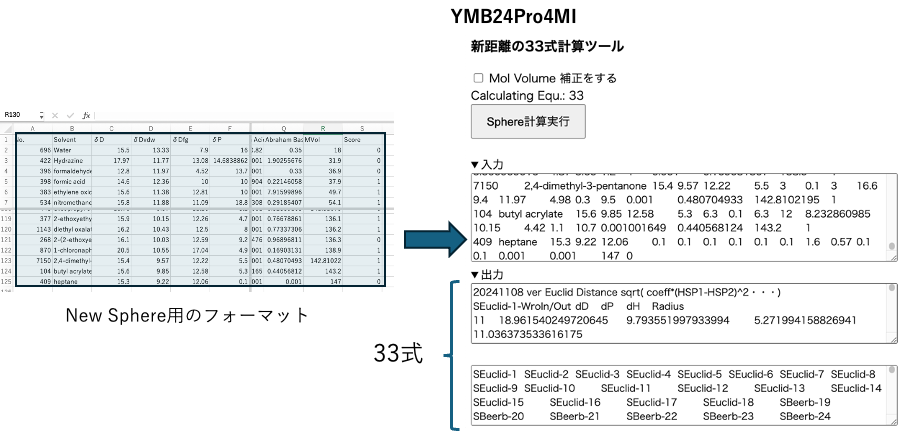
得られたデータセットを一旦Excelに戻し、再びコピーして次には、新距離の33式計算ツールの入力部分にペーストし、Sphere計算実行を行います。(計算に時間がかかるため、YMB24Pro4MIとは分離して単独実行のアプリになっています。CPUコアを5つ並列に使う設定になっています。)結果をExcelに戻します。
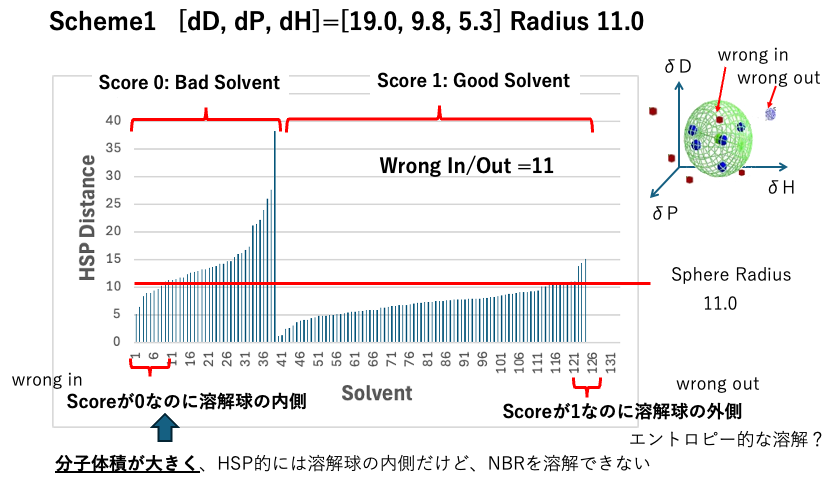
Scheme 1 は最もシンプルなHSP距離の式になります。
Scheme1 [dD, dP, dH]=[19.0, 9.8, 5.3] Radius 11.0
127データのうち、Scoreが0(貧溶媒)なのに球の内側に来たもの8つ、Scoreが1(良溶媒)なのに球の外に来たもの3つがありました。
Scoreが0(貧溶媒)といった時に、例えば溶媒の分子量がとても大きく(可塑剤のような)HSP的には溶解するはずだが、分子が大きすぎて内部に侵入できないことは良くあります。逆に良溶媒なのに球の外に来るものは解釈が難しいです。エントロピー的な溶解であるとか言われますが、HSP依存では無い溶解の場合もあります。(その為に33式に拡張して検討を行っている)
分子が大きいものは溶解しにくいという前提に立つなら、MVol補正をかけて計算することもできます。
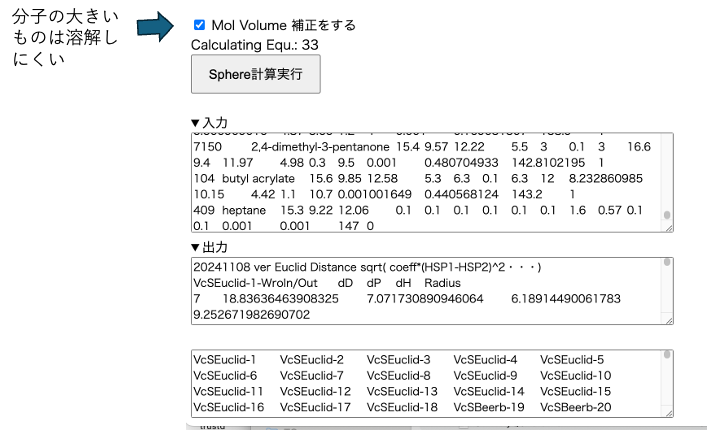
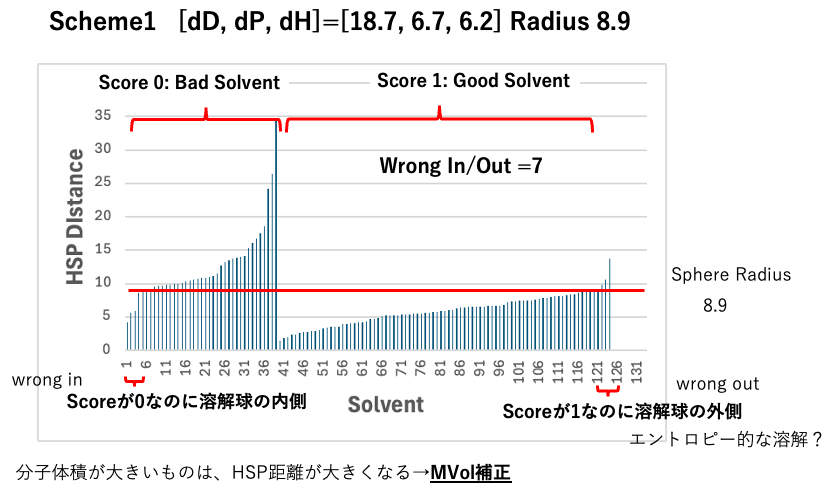
さらに誤認識は減りました。

このように、新しいツールを使うことによって、より短い半径で誤認識の少ないNBRのHSPを求めることができました。
NBRのHSPが決まったので、次はこのNBRとガソリン/エタノールの混合溶媒のHSP距離を検討します。
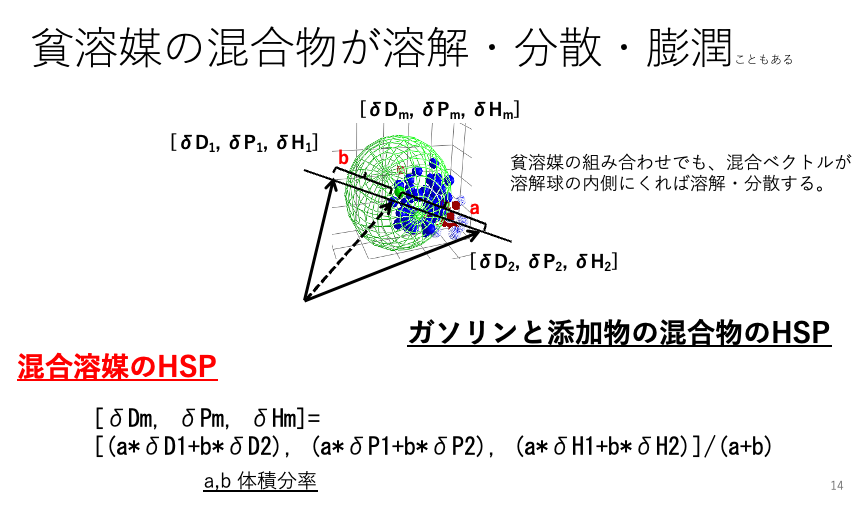
クラッシクな方法では、混合溶媒のHSPは単品のHSPと混合体積から計算で算出します。
先に求めた3種類のNBRのHSPと混合溶媒のHSPからHSP距離を計算します。アルコールの濃度が異なればHSP距離は変わるのですが、どの系でも、だいたい45%EtOH濃度でHSP距離が一番短くなります。豊田合成の論文では膨潤度最大とHSP距離最小値がほど一致と書いてありますが、軸のアサインが正しくないので、今回やり直したものの方が正しいと思われます。
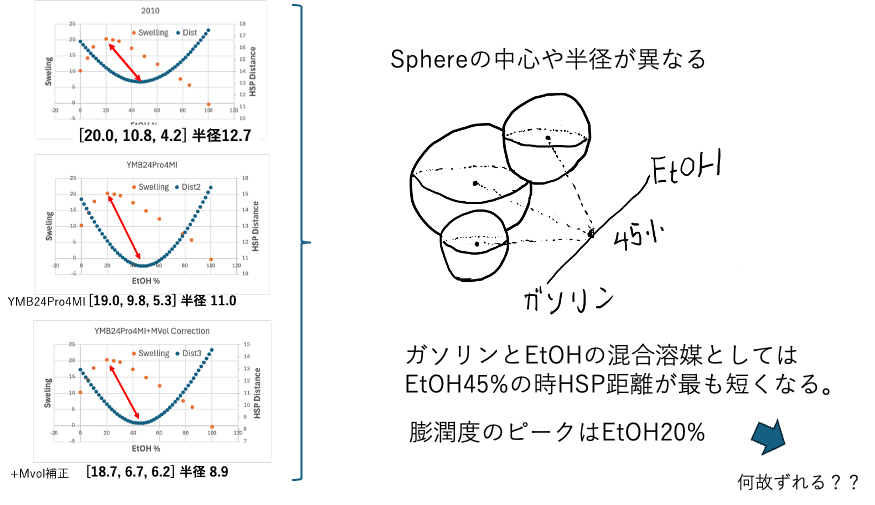
そこで何故ずれるか考えることが重要になります。
そんな時に、「新しい機能膜」という古い書籍から食品用のバリアフィルムのバリア機構が書いてある部分を見つけました。
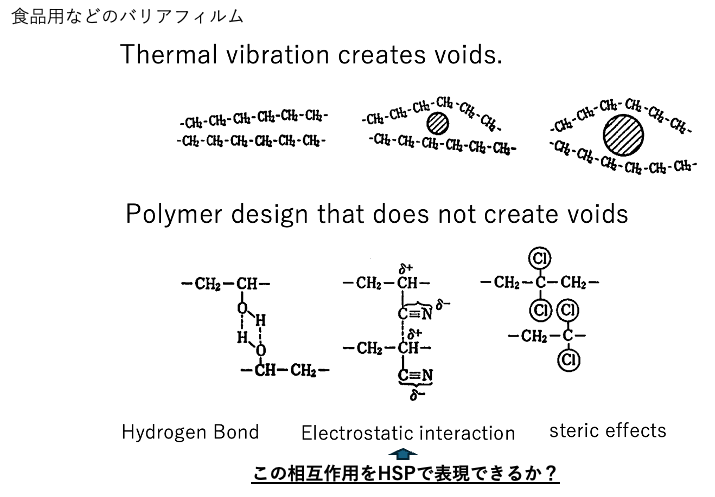
ニトリル・ポリマーのガスバリア‐性は、静電相互作用によるものだとされています。この効果がHSPに取り込まれているか考えてみます。
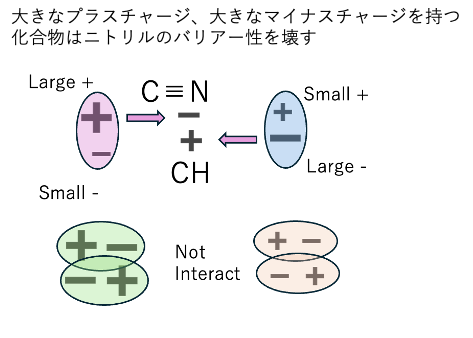
弱酸と弱塩基の塩に、強酸や強塩基を加えると交換反応がおこります。強酸と強塩基の塩に弱酸や弱塩基を入れても何も起きません。これを正しく判定するにはHSPの拡張が必要になります。
わたしは2017年のHSP50周年記念講演会でキーノートスピーチを2つ行いました。
まず1つめはdDの分割です。

つぎはdH項の分割です。

これらの拡張を元に距離の式を作ると全部で33種類になります。

33式の中で、どの式がどう効果があるかはやってみないと解りません。そこで片っ端から係数を定めてみます。
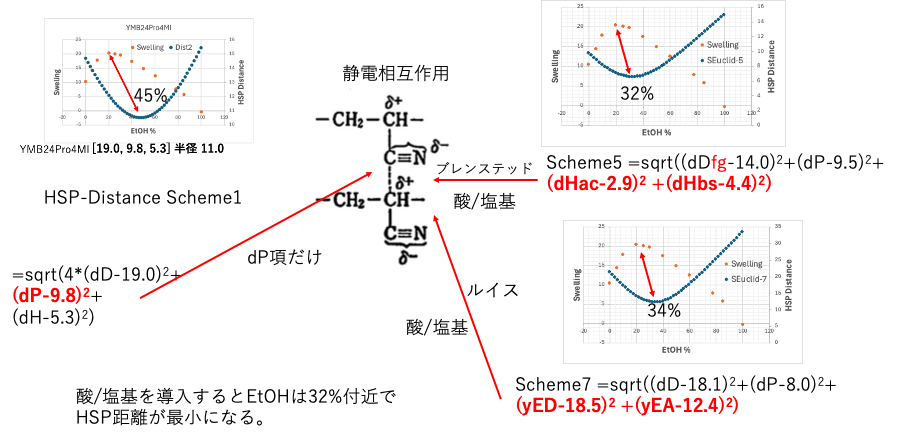
dHを分割しない時には、EtOHが45%でHSP距離は最小になりました。しかしブレンステッド、ルイスの酸塩基に分割したものはEtOH32%あたりが最短になりました。随分改善されます。
他の論文ではガソリンとメタノール混合溶媒のアクリロニトリル・ゴムの膨潤度が検討されていました。
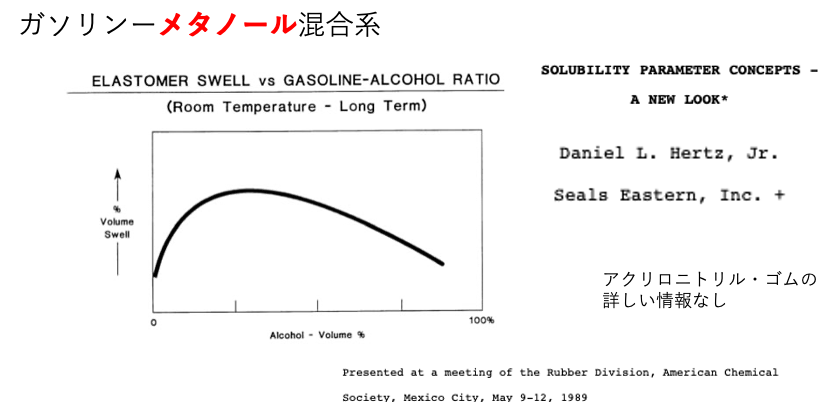
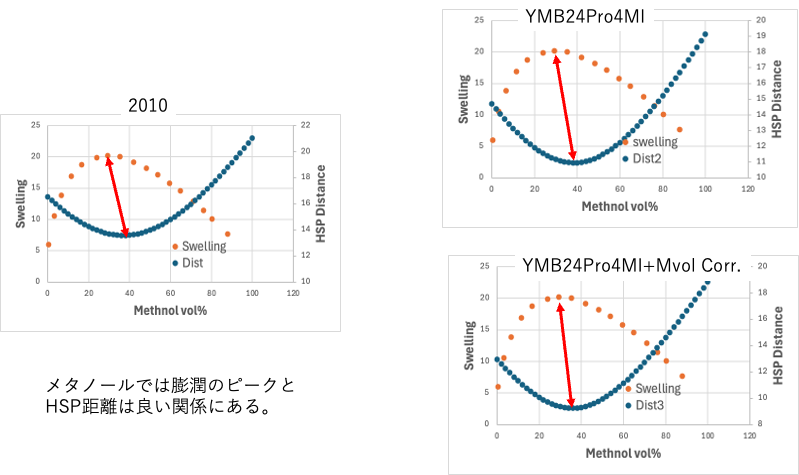
この場合はかなり良い一致が見れれます。
フッ素ゴムであっても、ガソリン/エタノールの混合燃料には膨潤しやすい事が知られています。ちなみに、このグラフにあるNBRが膨潤のピークはEtOH25%ぐらいになりそうです。
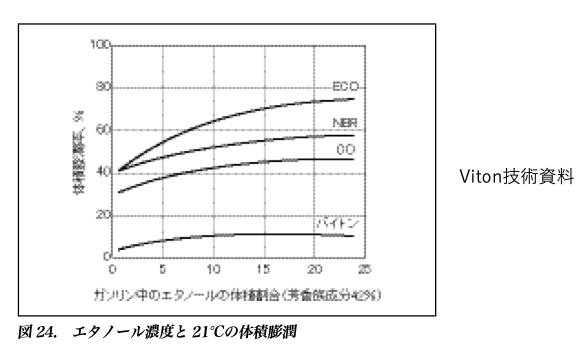
そこでFKMというフッ素系パッキンの耐溶剤性のデータを集めました。
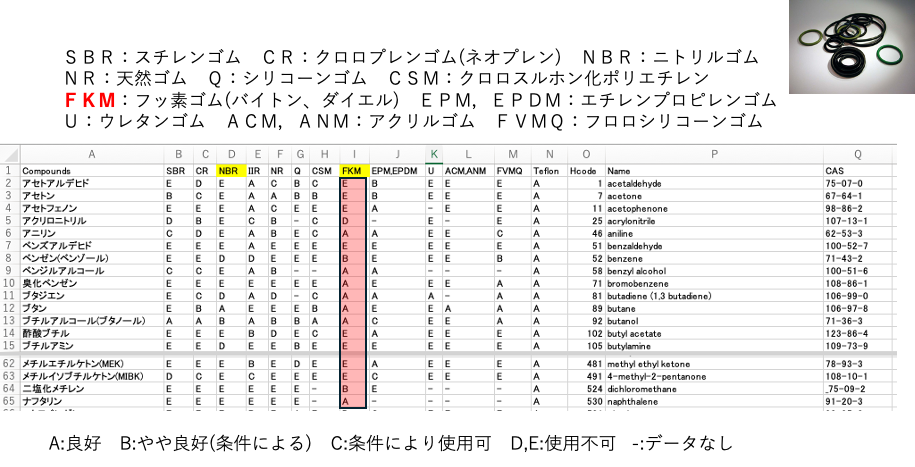
96種類の溶剤評価からテーブルが得られました。
また別途、ダイエル技術資料(ダイキン)には膨潤度の実データが記載されていました。
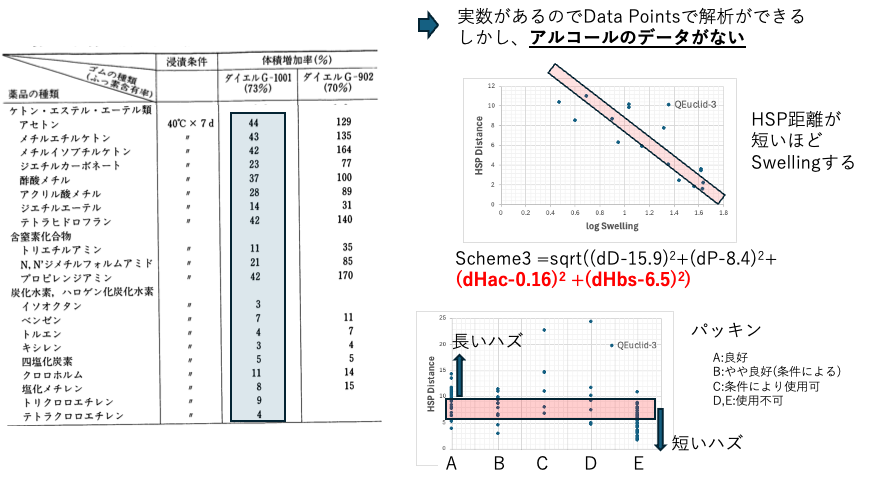
実データがあると、定量的な解析を行うことができます。HSP距離と実データがなるべく高い相関係数となるようにHSPの中心を求めます。この例では、式3のHSPを[dD, dP, dHac,dHbs]=[15.9,8.4, 0.16, 6.5]とすると高い相関関係が得られることがわかります。しかし、こうして得られた式3のHSPを用いてパッキンでの耐溶剤性データにあてはめてみると、とても多くのハズレ(Wrong In/Out)が現れてしまいます。何故うまくいかないかというと、ダイエルのデータにはアルコールが一つもありません。多様性の低いもので作った式を広く拡張するのは難しいということです。
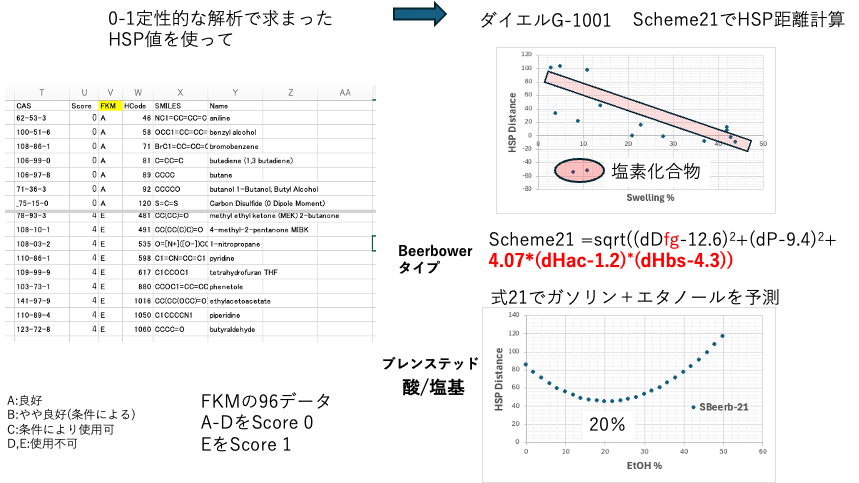
そこで、多様性の高い、しかし、定性的な0-1スコアから、33式のHSP中心を決めてダイエルの定量性のあるデータに適用してみます。塩素化合物2つが距離が非常に短いのに膨潤度は小さいという結果になりました。しかし、この式21でガソリン−エタノールの混合燃料を評価すると、Vitonのカタログと同じく、エタノール20%の時HSP距離が一番短くなります。
実はどの式が一番良いのかを判断するのはとても難しいことです。この場合はBeerbowerタイプの式でdHAc, dHbsに分けたものは皆下に凸になりました。(位置は少しずつ異なります)下に凸にならずに、下がり続ける式も多くあります。ダイエルのシール材で相関が高かったものが、混合燃料で良いピーク位置を与えるかといえば、逆のケースの方が多いです。
先に、EtOH20%の混合燃料に一番良く膨潤するという現象があった時に、それは、4.07*(dHac-1.2)*(dHbs-4.3)
に依存しているからという解釈をつけることはできます。しかし、何故式21で、塩素化合物のあいが悪いのかを考えるクセをつけるのが大事です。
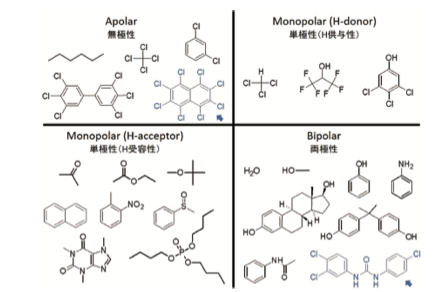
最近、環境化学(Journal of Environmental Chemistry)Vol.30, pp.145-150, 2020
環境有機化学実験における溶媒の選択
遠藤 智司先生の論文を読んでいて解った気がします。
Y-MB24Proでクロロホルムを計算すると、dHac=5.7, dHbs=0.1となります。
dHacが大きく、dHbsが小さい化合物は、4.07*(dHac-1.2)*(dHbs-4.3)が大きなマイナスになります。
両極性の化合物はアルコール、カルボン酸、アミン色々ありますが、単極性(H供与性)の化合物はとても少ないです。そこで、96化合物から距離の33式を作る際に、4.07*(dHac-1.2)*(dHbs-4.3)としてクロロホルムを除外しても大勢に影響が無いとプログラムが判断したのでしょう。
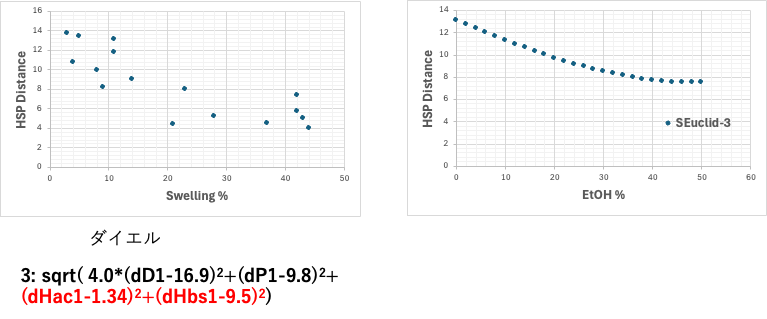
式3を使えば、塩素化合物の特異性は出ませんが、混合燃料の極値は大きくズレてしまいます。
任意の材料で混合溶媒にどのぐらい弱いかを予測することはとても困難です。
大まかには、
1: sqrt(4.0*(dD1-dD2)2+(dP1-dP2)2+(dH1-dH2)2)
3: sqrt( 4.0*(dD1-dD2)2+(dP1-dP2)2+(dHac1-dHac2)2+(dHbs1-dHbs2)2)
7: sqrt( 4.0*(dD1-dD2)2+(dP1-dP2)2+(yED1-yED2)2+(yEA1-yEA2)2)
で評価するのが良いでしょう。
HSPが近いものがよく溶かす。それが基本原則です。
細かいところまで合わせ込もうとしたら色々細かいパラメータも存在するのでさらに改良した式も得られます。しかし、合わせこむよりも何故かを考えることのほうが大事です。
今後、様々な現象に33式を適用していくに連れ、もう少し式の意味が明確になっていくかもしれません。YMB24Pro4MIのユーザーは色々試してみて欲しいと思います。
Copyright pirika.com since 1999-
Mail: yamahiroXpirika.com (Xを@に置き換えてください)
メールの件名は[pirika]で始めてください。
