2022.9.3改訂(2009.8.31)
解析例トップ
HSP基礎トップページ
概要
溶解を扱う理論はたくさんあるが、HSPを使う理由は10ある。それを紹介する。
MOSCED,
UNIFAC,
Jouyban-Acree,
Yalkowsy,
MOD (Mobile Order and Disorder)
などだ。
それぞれに魅力的な特徴がある。我々は特にHildebrand教授のパイオニアとしての溶解度パラメータ(SP値)に関する研究は,非常に尊敬している。
彼の研究が無ければHansenの溶解度パラメータ(HSP)も無かっただろう。
しかし,現在は他の方法でなく,HSPを使う10の理由がある。
(この記事はVer. 3 の内容を含み,それ以下のバージョンでは使えない。)
1 HSPは完全にHildebrand(ヒルデブラン)の溶解度パラメータを含んでいる。
HildebrandのSP値はHansenのSP値と次のような関係にある。
Hildebrand SP2 = tot HSP2 = dD2 + dP2 + dH2
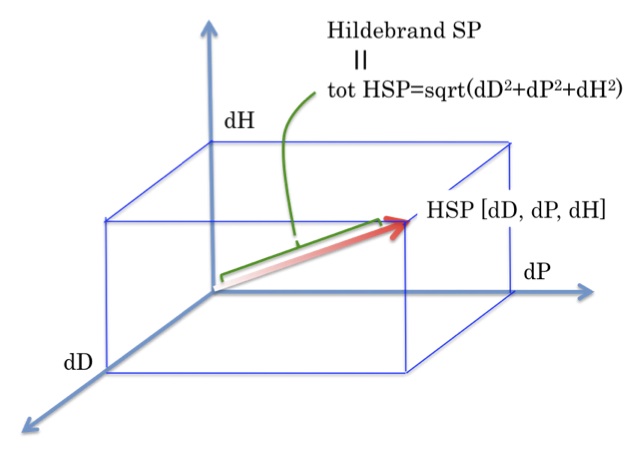
そこで、どうしてもヒルデブランの溶解度パラメータを使いたいのなら,tot HSPを使えばいいだけである。
HSPを3次元空間に[X, Y, Z]=[dD, dP, dH]としてプロットすると,HildebrandのSP値はそのベクトルの長さになる。
従ってHSPは完全にHildebrand SPを含んでいると言える。
そしてこの図から明らかなように,HildebrandのSP値の言う所は原点からの距離が同じになる球の表面を作るベクトルは皆同じ溶解性になると言っているのに等しい。
この原点はどういう意味を持つのかというと、蒸発潜熱が0になる点、すなわち臨界点を示している。
つまり溶解度パラメータは、化合物を比較するときに、臨界点からのベクトル距離で規格化している事になる。それはつまり対応状態原理と同じような考え方をしていることになる。
tot HSP=HildebrandのSP値が15.0になる化合物を我々のデータベースから選び出すと,71化合物あった。これらを3次元空間にプロットする。
Dragで回転、Shift-Dragで拡大・縮小、Option-Dragで移動
球をクリックすると溶媒の名称が表示される。
2009年の古い記述。
HildebrandのSP値が19±0.3になる化合物を我々のデータベースから選び出すと,391化合物あった。これらを3次元空間にプロットしてみよう。
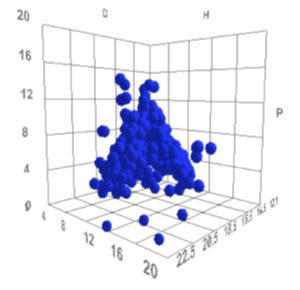
あるものはdDだけが大きく,dP, dHは小さい。
あるものはdDとdHが大きい。
あるものはdPが大きい。
しかし,これらは皆,原点[0, 0, 0]からの距離は15.0だ。
HSPの観点からはこれらの化合物は同じ溶解性を持つとは考えていない。
我々が“似たものは似たものを溶かす”と言った時には、我々の“似たもの”というのは、“似たベクトル”の事であって,原点からの距離の事ではない。
2 HSP は相互作用半径の概念を持っている。
(より詳細な記事はこちらのポリマーの溶解性を参照してほしい)
“ポリマーハンドブック”から,溶媒と貧溶媒の情報を得る事ができる。例えば,ポリ塩化ビニル(PVC)の良溶媒にはテーブル中でScoreに1を,貧溶媒にはScore 0を入れてある。
古いHSP Table
| name | dD | dP | dH | Score | tem | Vol |
| Chlorobenzene | 19 | 4.3 | 2 | 1 | 102.1 | |
| cyclohexanone | 17.8 | 8.4 | 5.1 | 1 | 104.2 | |
| cyclopentanone | 17.9 | 11.9 | 5.2 | 1 | 89.1 | |
| DMF | 17.4 | 13.7 | 11.3 | 1 | 77.4 | |
| DMSO | 18.4 | 16.4 | 10.2 | 1 | 71.3 | |
| MEK | 16 | 9 | 5.1 | 1 | 90.2 | |
| nitrobenzene | 20 | 10.6 | 3.1 | 1 | 102.7 | |
| THF | 16.8 | 5.7 | 8 | 1 | 81.9 | |
| 1,2-dichlorobenzene | 19.2 | 6.3 | 3.3 | 1 | 113 | |
| diisopropyl ketone | 15.6 | 6.7 | 4.1 | 1 | 140.2 | |
| dioxane | 17.5 | 1.8 | 9 | 1 | 85.7 | |
| ethylene chloroide | 18 | 7.4 | 4.1 | 1 | 79.4 | |
| isophorone | 17 | 8 | 5 | 1 | 150.3 | |
| mesityl oxide | 16.4 | 7.2 | 5 | 1 | 115.2 | |
| toluene | 18 | 1.4 | 2 | 1 | 106.6 | |
| acetone(SW) | 15.5 | 10.4 | 7 | 0 | 73.8 | |
| acetic anhydride(SW) | 16 | 11.7 | 10.2 | 0 | 95 | |
| EtOH | 15.8 | 8.8 | 19.4 | 0 | 58.6 | |
| aniline(SW) | 20.1 | 5.8 | 11.2 | 0 | 91.6 | |
| carbon disulfide | 20.2 | 5.8 | 0.6 | 0 | 60.6 | |
| Acetic Acid | 14.5 | 8 | 13.5 | 0 | 57.6 | |
| ethyl acetate | 15.8 | 5.3 | 7.2 | 0 | 98.6 | |
| hexane | 14.9 | 0 | 0 | 0 | 131.4 | |
| vinyl chloride | 16 | 6.5 | 2.4 | 0 | 64.7 |
このテーブルをtab区切りのテキスト形式で,拡張子をssdとして保存する。(最新のデータ・フォーマットは.hsdフォーマットである。 ver.5.4からはhsdxフォーマットしか扱えなくなった。)これはHSPiPから直接開くことができ,
次のデータからSphere計算用のhsdxフォーマットのデータを作ってみよう。
CAS番号は、Excelで勝手に変更されないように、日付になるものの前には”_”が挿入されている。HSPiPで検索するときには外す。
データが作成できたら、Sphere計算ボタンを押すだけでPVCのHSPをたちどころに計算する。
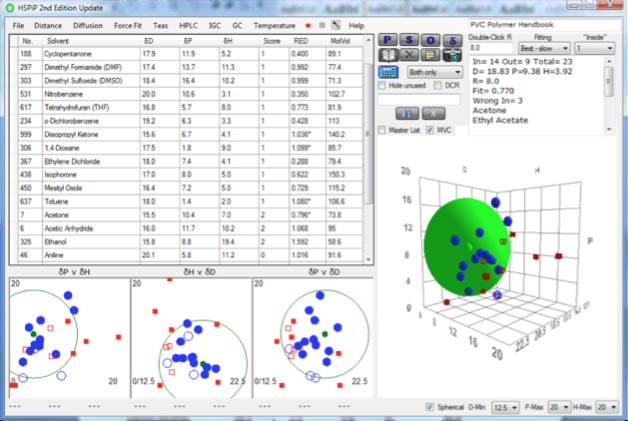
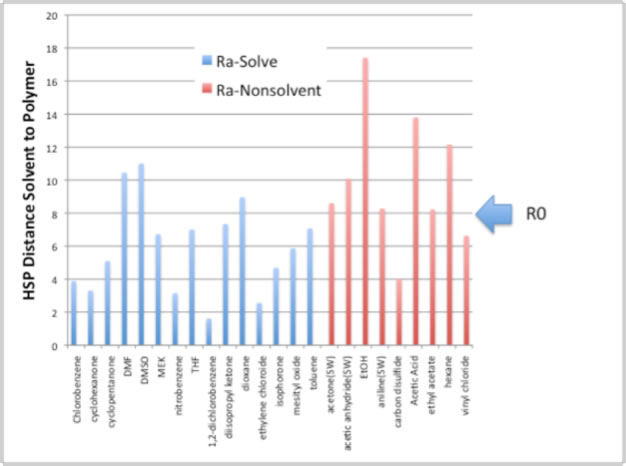
PVClを溶解する溶媒からSphereをプロットすると下のような関係になる。
このプロットは、溶解試験を行った溶媒のHSP[δD, δP, δH]を3次元空間にプロットしたものだ。
小さな球(溶媒)をクリックすれば溶媒の名前が現れる。
Drag=回転, Drag+Shift キー=拡大、縮小, Drag+コマンドキーかAltキー=移動。
緑色の大きな球は、ハンセンの溶解球と呼ばれるものだ。
赤い球は先ほどのテーブルで良溶媒と設定された溶媒で、そして青い球は貧溶媒と設定された溶媒だ。
良溶媒(赤い球)はハンセン空間中の似たような位置に集まっており、良溶媒を取り巻くように、緑のハンセンの溶解球が見つけ出されている。 大きな緑色の球の中心がPVCのハンセン溶解度パラメータ(HSP)となる。
大きな緑色の球の半径(R0)が良溶媒の限界になり、その半径を相互作用半径R0と呼ぶ。
PVCのR0は8.0になる。
各溶媒のPVCのHSPからの距離(Ra)を(セクション3に示す方法で)計算する。
相対的エネルギー差(RED)はRED=Ra/R0で表される。
これは,つまり,その溶媒が緑色の球の内側か外側かを示している。
我々の主張は、ポリ塩化ビニルの他の溶媒、混合溶媒を探索したいのなら、このハンセンの溶解球の中に入る(相互作用半径以下の距離を持つ)溶媒を探せば、見つかる可能性が高いという事だ。
実際にマウスをドラッグ(左ボタンを押したままマウスを動かす)してみよう。
赤い良溶媒なのに球の外に存在する溶媒がある。そうした溶媒をWrong outと呼ぶ。
分子の大きさなどによるエントロピー効果や、未知の相互作用などで、HSP的には溶解しないはずの溶媒が、実際には溶解することもある。
そうした発見は、新しいサイエンスとして深堀するテーマになりうる。
逆に(今回はそのような溶媒は見当たらないが)HSP的にはハンセンの溶解球の内側に位置しているのに、溶解しない(青い球で表示)Wrong inの溶媒が見つかる事がある。
PVClを溶解する溶媒が2種類あるとして、Sphereを2つ求めると上のような結果になる。
このDoubleSphere法は、ポリマー中に異なる溶解性を持つ領域が2つ存在すると仮定する。
ある溶媒が溶解するすると言った場合、その溶媒が領域1もしくは領域2のどちらかに含まれ、ポリマーを溶解しない溶媒は領域1,2のどちらにも含まれないような領域1と2の半径と中心点(HSP値)を求める技術である。
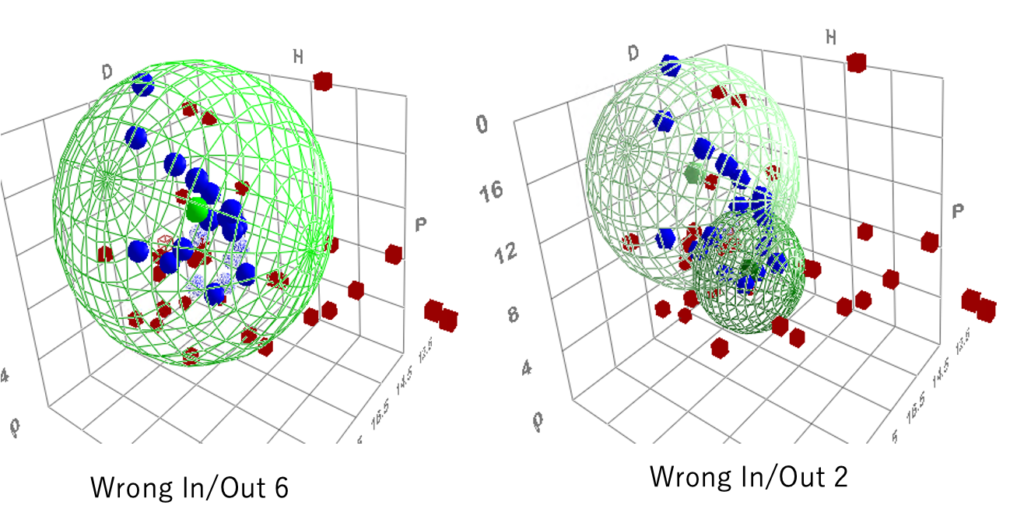
一般的には誤認識は減る。
実際にREDの意味をグラフで見てみよう。
(Sphereの求め方が異なるので、Wrong In/Outの数は上の説明とは少し異なる)
RED < 1 ならば溶媒と溶質は似ていて完全に溶ける。
RED = 1 ならば部分的に溶ける。
RED > 1 ならば溶けない。
溶媒とポリマーのHansenベクトル距離がRa>8であったならば,ポリ塩化ビニルを溶かさない。
そこで,DMF, DMSOとDioxaneは例外である。
そしてRa<8であるならポリマーを溶かすはずなので,2硫化炭素と塩化ビニルは例外である。
Ra<R0であるにもかかわらず溶解しないのには,いくつかの理由が考えられる。
例えば分子が非常に大きくてポリマーの中に入り込めないだとか,単に溶解するのに非常に長い時間を要しているだけかもしれない。
例えば可塑剤のように良く溶解する(溶け合う)が分子のサイズが大きすぎて、溶媒としては溶解できないこともある。
こうしたいくつかの例外はあるものの,現実的な観点から言って,この結果は溶媒探索に非常に効果的だ。
これをHildebrandのSP値でやろうとするとものすごく困ったことになる。
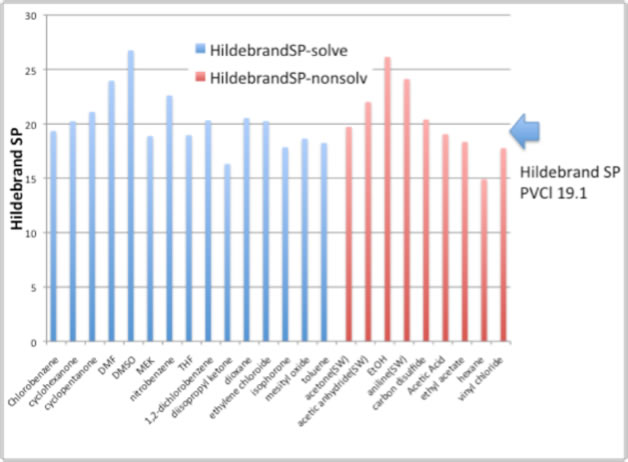
良溶媒と,貧溶媒でHildebrandのSP値はほとんど変わらない。
そこで、どれがPVCを溶解するかについては何も言えない。
残念ながら,他の溶解理論には球,相互作用半径(R0), HSPベクトル距離(Ra), 相対的エネルギー差(RED)の概念が無い。
そこで現実問題を扱う研究者に実際的な情報を与える事ができない。
3 HSPは多成分系を扱う事ができる。
他の溶解度の理論では溶媒の混合物を扱うのは容易ではない。
HSPでは混合溶媒を単なる“ベクトルのたし合わせ”として取り扱う事ができる。
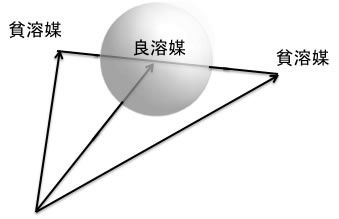
2つの貧溶媒を混ぜると良溶媒になるという多くの例題がある。
例えばPMMA[17.7, 9.1, 7.1 ]はブタノール[16.0, 5.7,15.8 ]にも硫化ジエチル [16.8, 3.1, 2.0]にも溶けない。
青いベクトルも赤いベクトルも緑の球の中心からはとても離れているのが簡単に分かるだろう。
しかし50:50の混合溶媒のベクトルは. [16.4, 4.4, 8.8]になり,緑の球の中心にとても近くなり,そして事実この混合溶媒はPMMAを溶かした。
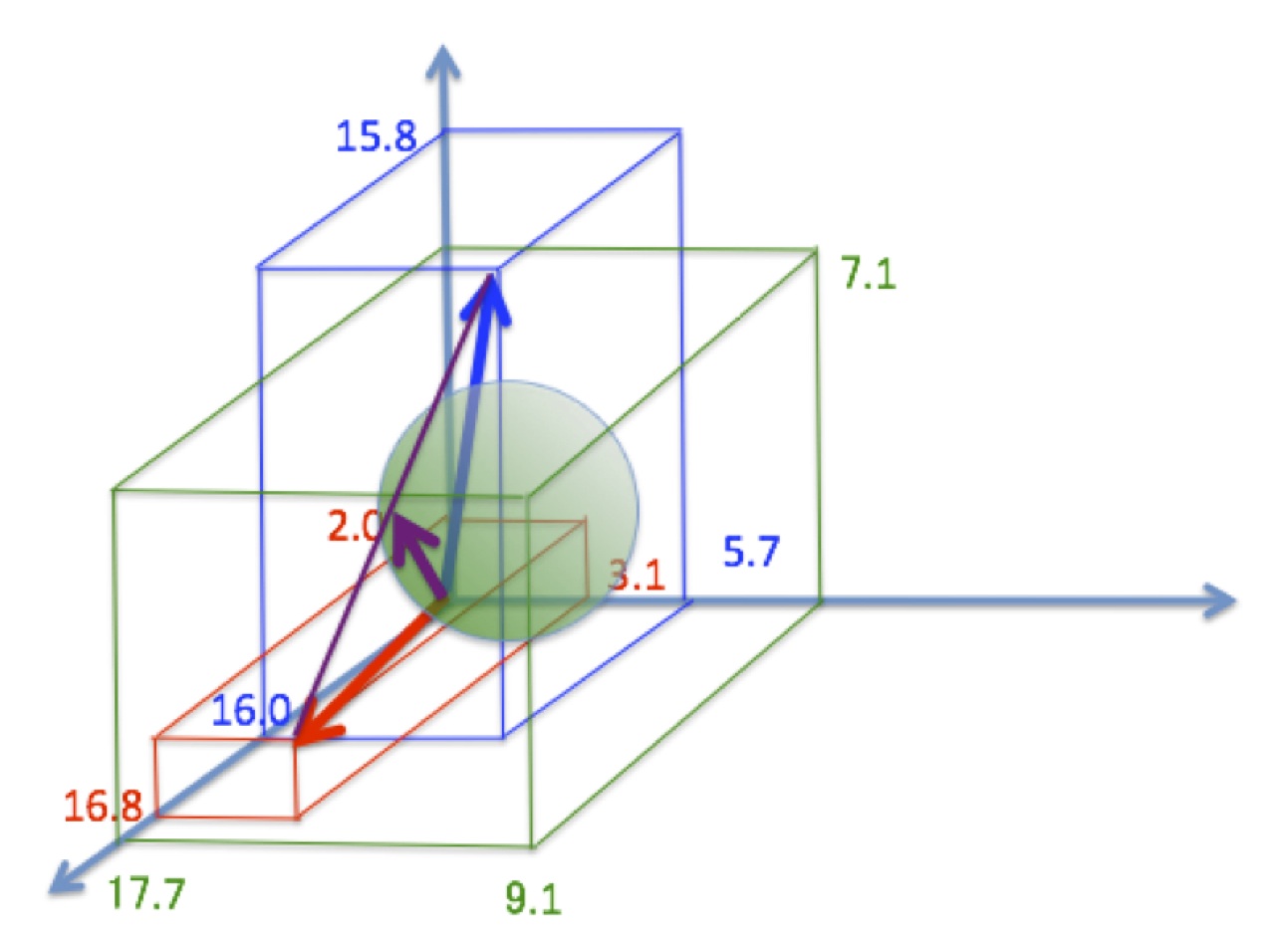
2011.4.22
実際にこの例をプロットしたものである。
Drag=回転, Drag+Shift キー=拡大、縮小, Drag+コマンドキーかAltキー=移動。溶媒をクリックすれば溶媒の名前が現れる。
溶媒はどちらも緑色の球の外側にあるので単独では溶解しない。
しかし、2つの溶媒を線で結ぶと緑色の球と交差するのが判るだろう。
この事は初期にはHSPのコンセプトの証明となり,HSPを使う良い理由になった。
しかし,現在は2元系にHSPを使うさらに良い理由がある。
それは,活量係数や,ヘンリー定数,Margulesパラメーター,共沸などが新しいHSPiPで使えるようになったからだ。
4 HSP は溶解しない溶解度を扱う事ができる。
(関連する記事はこちらのグラフェンの溶解性の記事を参照して欲しい)
基本的には溶解度パラメータは蒸発潜熱によって決定される。
そこで蒸発しないものの溶解度パラメータは直接決める事はできない。
例えばイオン液体は蒸気圧を持たないので溶解度パラメータを直接決める事はできない。
しかし,セクション2で説明したテクニック(いわゆる挟み撃ち法)を使ってHSPを決める事ができる。
我々はナノカーボン,顔料,ガラスのHSPを使う事ができる。
HildebrandのSP値でも溶解しないもの(蒸発しないもの)の溶解度パラメータを扱う事ができるという反論があるかもしれない。
例えばC60の溶媒に対する溶解度が調べられた。
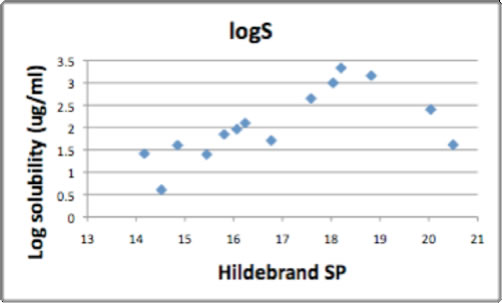
結果を見るとHildebrandのSP値と良い相関があるように見える。
そしてこの論文の作者はC60のHildebrandのSP値は18.4であると結論づけた。
しかし,数年経って他の研究者が他のデータを発表した。そうしたデータを全てプロットして見ると非常に困ったことになってしまう。
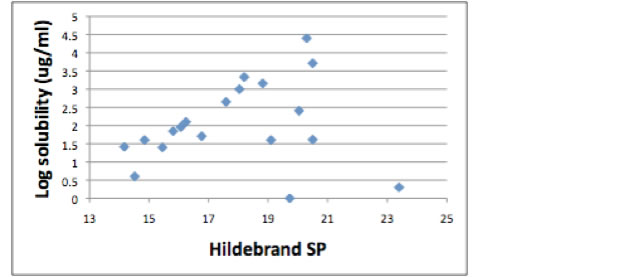
トップピークの位置は20.3 (25000ug/ml)にずれてしまい,しかもピークに近いHildebrand SP=19.7の溶媒が1ug/mlしか溶解しない事が分かった。
つまり,非常に限られた範囲の溶媒だけなら,それなりに相関が見られるが,非常に広い範囲の溶媒に適用すると矛盾をきたしてしまう。
(セクション1を読んでいれば理由はお分かりだろう)
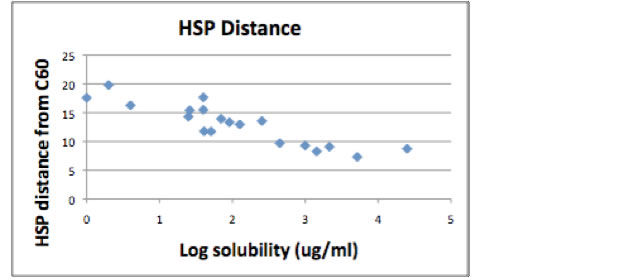
HSPiPのSphere機能を使ってC60のHSPを決定すると,[20, 3, 2]になり,上に示した溶媒とC60とのHSP距離をLog(溶解度)に対してプロットすると下図のようになる。
2011.4.22
Drag=回転, Drag+Shift キー=拡大、縮小, Drag+Shift キー=拡大、縮小, Drag+コマンドキーかAltキー=移動。溶媒をクリックすれば溶媒の名前が現れる。
dDを22にするとさらにフィティングはよくなるが,dDが20でも全体的な傾向は変わらない。
この図を見ると,“ベクトルの距離が短い=良く溶解する”という関係が簡単に見て取れる。
細かいことを説明すれば,我々がHSP距離という時には次の式を使う。
Ra = sqrt(4*(dD1-dD2)*(dD1-dD2)+(dP1-dP2)*(dP1-dP2)+(dH1-dH2)*(dH1-dH2))
dDの前に4がついている事に注意して欲しい。
その理由を簡単に説明するのは難しいが,HSPでは重要な値だ。詳しくはユーザーハンドブックかe-Bookを参照して欲しい。
5 HSPはオフィシャルのデータベースを持つ。
我々は1200以上の化学品,600以上のポリマーのオフィシャルなHSP値のデータベースを持っている。
それに加え,6000超のY−MBで計算されたHSP値のデータベースを持っている
(第4版では10000超となった。第5版ではポリマーDB が1400超になった)
我々はさらに香料のデータや2元系のデータなどを収集している。そして,我々の推算精度を高く保つ為に,その値を一つ一つ吟味している。こうしたデータを集積している時に,我々は市販のデータベースやハンドブックに間違いがある事に気がついた。ここに示すのはHildebrand SPが矛盾しているものの一部を示した。
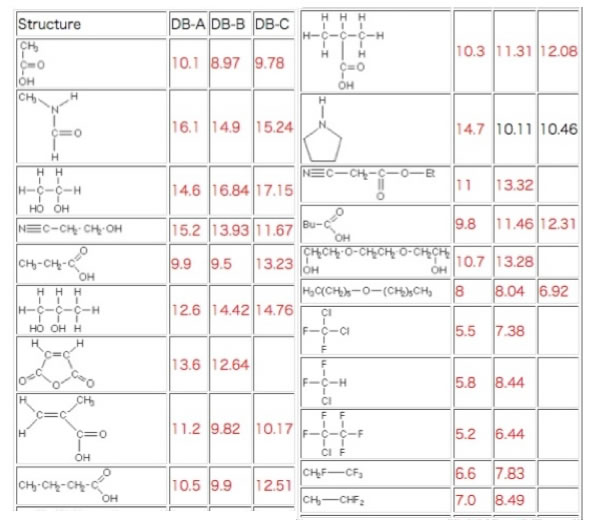
DB-A, DB-B, DB-C はそれなりに有名なデータベースで多くの研究者が使っていると思う。
しかしHildebrand SP値(単位は(cal/mol)^0.5 )は例えばカルボン酸化合物や,ハロゲン化合物で値が一致しない。あなたならどの値を信じるだろうか?
Hildebrand SP 値は簡便で広く使われているがオフィシャルな値が無い。
何か問題があった時に,原報にさかのぼって膨大な調査をしなければならない。
6 HSPにはオフィシャルな文書とソフトウエアー,“HSPiP”がある。
HSPにはオフィシャルな文書 “Hansen Solubility Parameters A User’s Handbook”と”HSPiP e-Book”があり,そしてオフィシャルなソフトもある。
HildebrandのSP値には正式でない多くの文書とソフトウエアーがある。
しかし,セクション5で指摘したように,同じ化合物でも様々な値が割り振られているので,計算値であっても,その計算式を作るのに使ったデータがどれを使ったかによって結果も大きく変わってしまう。
すると他の研究者の結果をトレースしようとしても彼らがどのソフトウエアーのどのバージョンを使ったかが分からないとどうしようもないことになる。
我々はオフィシャルの文章,ソフトウエアーを日々更新している。
もしかすると,すぐに新しいバージョンになるので,今買わなくても良いのではないかと思うかもしれない。
しかし,買うなら今が良い。
なぜなら,我々はユーザーのニーズを第一優先に考えているからだ。
我々はソフトウエアーの更新をユーザーの要求に答えるように,そしてHSPコミュニティー全体が利益を享受できるように行う。
既存のユーザーは無料でアップグレードできるが,新規のユーザーの値段は少し高くなっている。
7 HSP は実際の現場に使われている。
溶解性が等しいだけで,ある溶媒から他の溶媒へ切り替えられるだろうか?
溶解度パラメータは溶解以上の事に言及しない。
しかし,現実の世界では,例えば,インクや塗料の新しい溶媒を設計しようとした時には沸点は非常に重要になる。
揮発油と同じ溶解性を持ち,環境や健康に問題のない溶媒であっても乾燥するのに1ヶ月かかる絵の具だったら誰が使おうと思うだろうか?
我々のHSPiPは現実世界の溶媒を取り扱う総合システムだ。
我々は顧客が必要とする機能をどんどん付け加え続けている。
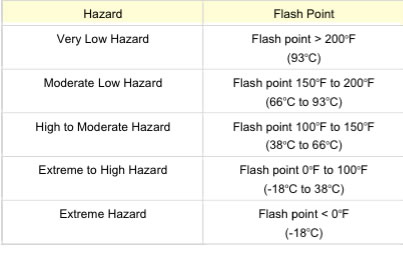
溶媒に対して最も重要な物性値は引火点であろう。
危険物の分類は引火点による。
HSPiPは引火点だけでなく、水酸基ラジカルとの反応性(大気寿命)MIR(Maximum Incremental Reactivity:大気中揮発性有機化合物[VOC]のオゾン生成能)= VOC 変化量当たりの最大オゾン変化量,蒸気圧,分配係数などを推算する。
他のどの溶解度の理論もこれらの機能を搭載しておらず,実際の現場では使い物にならない。
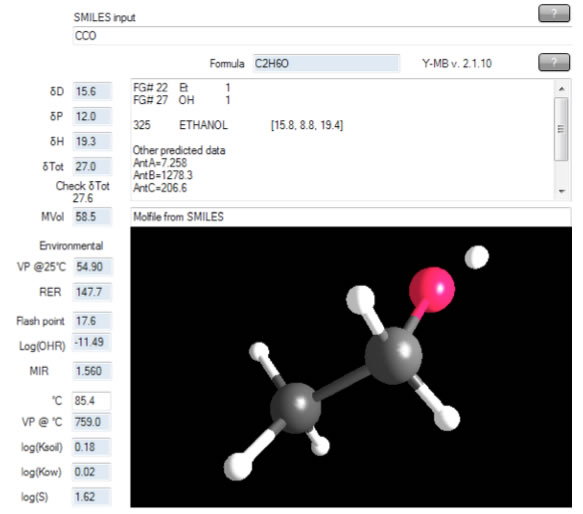
8 HSP は他の科学と相乗効果がある。
(関連する記事はHPLCの保持時間を参照して欲しい)
HSPは科学であり,科学は他の科学と相乗効果を持つ。
HSPもっとも重要な相乗効果の一つは分析化学のクロマトグラフィーのリテンションだ。
インバース・ガスクロ(IGC)からHSPの実験値を計算できる。
そして,HSPの値からガスクロのリテンションインデックス(GCRI)やHPLCの保持時間を予測する事ができる。
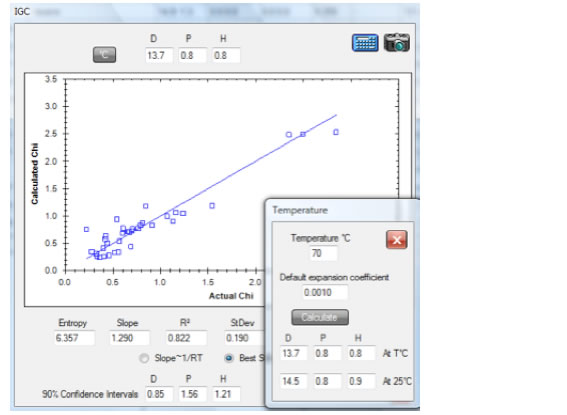
化学工学,薬学、毒性学,動物学,匂いや味の分野とも相乗効果をあげつつある。
9 HSPは多様性がある。
溶解度の理論はたくさんあるが,特殊な応用の狭い分野の事柄に,小さな研究グループだけが使っているという傾向がある。
HSPだけが非常に広い範囲の応用に対して使われている。
ここに現在のe-Book(V5.3の章立て)の内容を示そう。
HSPがいかに広い分野に使われているかお分かりいただけるだろう。
またe-Bookの内容は版が上がるたびにどんどん増えている。
Introduction & Guarantee by Steven Abbott……………………………………………. 5
スティーブン・アボットによる緒言と保証
Chapter 1 The Minimum Possible Theory (Simple Introduction) …………… 11
最小限の理論。
Chapter 2 The Sphere (The Preferred Method of Visualizing)………. 16
Sphere(球)
Chapter 3 Your first HSP Sphere (Determining the HSP Sphere)…………… 19
最初のハンセン溶解球(Sphere)
Chapter 4 The Grid (A different route to the Sphere) ……………………………….. 26
グリッド
Chapter 5 FAQ – The Radius and other questions…………………… 29
よくある質問
Chapter 6 Coming clean (Finding Good Solvents) ………………………. 35
きれいになる
Chapter 7 Safer, Faster, Cheaper (Optimizing Solvent Formulations) ….. 40
安全に、早く、安く
Chapter 8 Coming together (Polymer Compatibility)………………………………….. 42
ご一緒に
Chapter 9 Sticking, Flowing and Dissolving (HSP and Adhesion, Viscosity and Dissolving) …………………. 45
接着、流れ、溶解
Chapter 10 Polymer Miscibility ……………………………………….. 61
ポリマー同士の溶解
Chapter 11 Shades of Black (Designed Partial Compatibility – Bitumen)…. 68
黒い陰
Chapter 12 Insoluble solubility parameters (HSP for Pigment Surfaces)……….. 72
溶けない溶解度パラメータ
Chapter 13 Cracks in the system (Environmental Stress Cracking) ………… 76
クラックが入る
Chapter 14 Let’s make this perfectly clear … (Formulating clear automotive lacquers)… 82
完全に透明な被覆を作ろう
Chapter 15 That’s swell (HSP and Swelling) …………………… 87
それは膨潤だ
Chapter 16 Paint failure – the science of blistering ……………………. 90
塗装の失敗ー水ぶくれの科学
Chapter 17 Skin deep (HSP and Skin Absorption) ……………………… 94
お肌の奥深く
Chapter 18 HSP and Diffusion…………………………………………………. 103
HSPと拡散
Chapter 19 It’s your call (Rational Selection of Chemical Protective Gloves) .. 122
あなたが決めてください
Chapter 20 Gloves: from minimum data to maximum insight (Exploring Glove Permeation).. 128
手袋:最小限のデータから最大限の洞察を得る
Chapter 21 Saving the planet (Finding Improved Environmental Solutions)…. 148
地球を救え
Chapter 22 HSP for ionic liquids (How to Assign HSP to New Materials) …….. 157
イオン液体のHSP
Chapter 23 Cleaning by numbers (HSP for Surfactants) ………………… 168
指標による洗浄
Chapter 24 Chromatography – HSP creator and user (Retention Times and HSP)…………………………………. 172
クロマトグラフィー、HSP値を決めたり使ったり
Chapter 25 Noses artificial and natural (HSP for Sensors Both Artificial and Live) ………………………………. 187
人工の鼻、自然の鼻
Chapter 26 Attacking DNA (HSP for DNA , Drugs, and Biological Membranes Compared)………………….. 198
DNAへの攻撃
Chapter 27 HSP for Pharma and Cosmetic applications………………………………… 204
医薬品と化粧品への応用
Chapter 28 Exploring with HSP – (Generating and testing research hypotheses)…… 206
HSPを使って探究する
Chapter 29 Liquid extraction – a work in progress……………………………… 210
液体抽出
Chapter 30 The HSP of gel formation……………………………………………………. 213
ゲル形成
Chapter 31 Going nano (HSP Characterizations of Nanoparticles)……….. 220
ナノ最前線
Chapter 32 DIY HSP (Methods to Calculate/Estimate Your Own HSP) ….. 230
自分でやってみよう
Chapter 33 Predictions (Many Physical Properties are Correlated with HSP) ……. 239
予測
Chapter 34 Improvements? ……………………………………………. 244
改良
Chapter 35 Into the 4th Dimension. Donor/Acceptor ……………….. 246
4次元へ。ドナー/アクセプター
Chapter 36 QSARs ………………………………………………………… 251
定量的活性相関
Chapter 37 SFBox-FE …………………………………………………………. 263
SFBox Scheutjens-Fleer(SF)理論
Chapter 38 A Short History of the Hansen Solubility Parameters……….. 273
ハンセン溶解度パラメータの歴史
Chapter 39 The next steps (What Is Planned and Asked For) ………….. 282
次のステップへ
10 HSPはAbbott, Hiroshi そしてHansenによって開発が続けられている。
HSPはただ一つの統一的な,広い範囲に使える理論で,しかもいまだに精力的に開発が続けられている理論だ。
我々は最初の版を去年(2008年)の12月に、(2009年)3月には第2版を,6月にはそのアップデートを出した。
]今我々は第3版を準備(2010年リリース)している。 2022年にはver.5.4をリリースした。
我々はプログラムやデータを改良している。
我々は新しい機能を付け加えている。そして我々は現実問題を解決するための手段を顧客に提供し続ける。
(バージョンアップ履歴)
解析例トップ
HSP基礎トップページ
Copyright pirika.com since 1999-
Mail: yamahiroXpirika.com (Xを@に置き換えてください)
メールの件名は[pirika]で始めてください
