2022.9.9改訂(2010.3.26)
解析例トップ
HSP基礎トップページ
分析関係トップページ
概要
カルボン酸は溶解度パラメータの中でも困り者の化合物だ。
HPLCの一斉分析のデータを入手したので、HSPを使ってリテンション・タイムとの相関を検討した。
また、蒸発潜熱のデータから、カルボン酸が困り者になる理由を説明する。
内容
ハンセンの溶解度パラメーの研究をしていると、カルボン酸化合物はいつも困りものだ。
HSPが似たものは似たものを溶かす。そう考えたときに、他のものではよく合うのにカルボン酸化合物は例外になりやすい。
データの入手
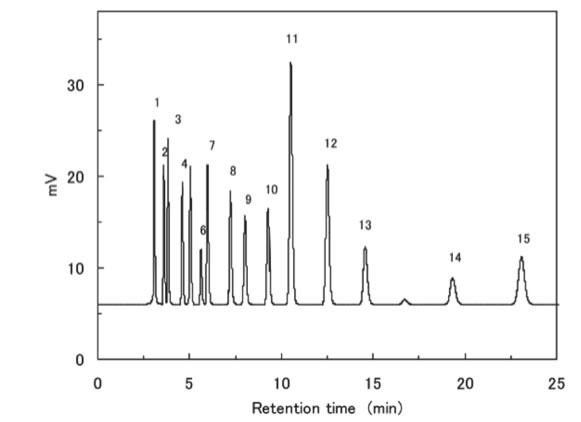
カルボン酸化合物のHPLCのデータを入手した。
テーブル
| No | name | RT |
| 1 | oxalic acid | 3.068 |
| 2 | L-tartaric acid | 3.579 |
| 3 | formic acid | 3.831 |
| 4 | L-malic acid | 4.597 |
| 5 | L-ascorbic acid | 5.002 |
| 6 | lactic acid | 5.622 |
| 7 | acetic acid | 5.967 |
| 8 | maleic acid | 7.191 |
| 9 | citric acid | 8.008 |
| 10 | succinic acid | 9.279 |
| 11 | fumaric acid | 10.475 |
| 12 | acrylic acid | 12.471 |
| 13 | propionic acid | 14.53 |
| 14 | glutaric acid | 19.278 |
| 15 | itaconic acid | 23.037 |
データをコピペしてY-MBのバッチ処理を使って、HSPを計算しておこう。
これらの化合物のHSPの推算値から、HPLCのリテンションタイム(RT)予測式の作成を行った。
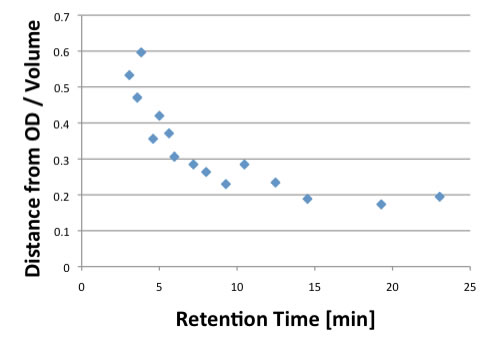
オクタデカン(OD)からの各カルボン酸のHSP距離を計算し分子体積で割り、それをリテンションタイムに対してプロットすると上図のようなかなりきれいな相関が得られる。(縦軸をlogを取るとほぼ直線になる。)
これらの化合物のHSP値をハンセン空間にプロットしてみる。
Drag=回転, Drag+Shift キー=拡大、縮小, Drag+コマンドキーかAltキー=移動。
青い球をクリックすれば酸の名前が現れる。緑色の球はオクタデカンを示す。
オクタデカンに近いものはよく溶解しRTが長くなると判断される。
この結果は非常にリーズナブルに思えるが、自分にとっては非常に不思議だ。その理由を説明しよう。
ここで用いたのは、HSPの推算値だ。(オリジナルの記事は2010年に書いたものなので、計算値はY-MB3.0辺りの古い計算値になる。上記のSmilesの構造式を用いて最新のY-MBで計算し直してグラフを作り直してみよう。)
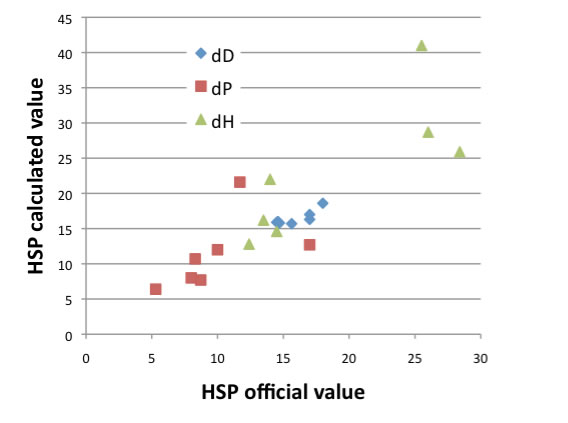
上の図はカルボン酸化合物のオフィシャルなデータベースの値と、その推算値をプロットしたものだ。(この計算も古いものなので計算しなおそう)
これを見ると、推算精度はあまり高くない。溶解度パラメータは蒸発潜熱をベースに理論が構築されている。そこで、低分子のカルボン酸のように、水素結合を作りダイマーで蒸発する化合物は推算が難しい。
| Official Value | Calculated Value | ||||||
| No | Name | dD | dP | dH | dDMR | dPMR | dHMR |
| 1 | oxalic acid | 17 | 17 | 26 | 17 | 12.7 | 28.7 |
| 2 | L-tartaric acid | 17.3 | 15.5 | 40.3 | |||
| 3 | formic acid | 14.6 | 10 | 14 | 16 | 12 | 22 |
| 4 | L-malic acid | 17.1 | 12 | 30.1 | |||
| 5 | L-ascorbic acid | 18 | 11.7 | 25.5 | 18.6 | 21.6 | 41 |
| 6 | lactic acid | 17 | 8.3 | 28.4 | 16.3 | 10.7 | 25.9 |
| 7 | acetic acid | 14.5 | 8 | 13.5 | 15.9 | 8 | 16.2 |
| 8 | maleic acid | 16.9 | 10 | 22 | |||
| 9 | citric acid | 17.9 | 9.3 | 31.3 | |||
| 10 | succinic acid | 16.9 | 8.3 | 19.3 | |||
| 11 | fumaric acid | 16.9 | 10 | 22 | |||
| 12 | acrylic acid | 15.63 | 8.72 | 14.5 | 15.7 | 7.7 | 14.6 |
| 13 | propionic acid | 14.7 | 5.3 | 12.4 | 15.8 | 6.4 | 12.8 |
| 14 | glutaric acid | 16.6 | 8.9 | 16.5 | |||
| 15 | itaconic acid | 16.6 | 8.4 | 18.1 |
蒸発潜熱の推算の理論
蒸発潜熱と沸点の間には、Troutonの通則というものがあり、非極性の化合物であれば
Lb/Tb=21 cal/g-mol
という関係があることが知られている。この場合の蒸発潜熱は沸点における蒸発潜熱であるが、容易に25度へ拡張できる。
試しに、化合物の沸点と25度での蒸発潜熱をプロットすると下のようになる。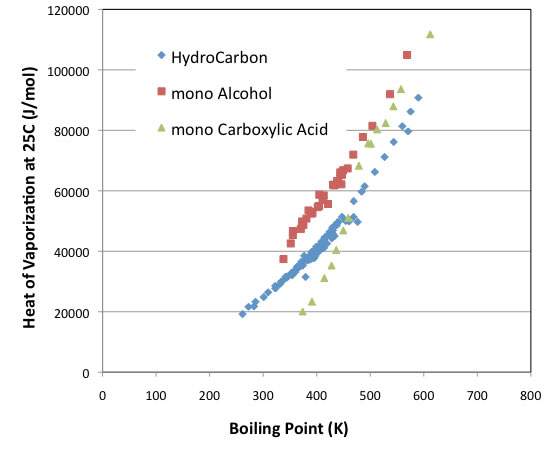
化合物の種類によって切片は異なるが、だいたい平行な曲線になる。
例外はカルボン酸化合物で、沸点が480Kを超えるようなカルボン酸化合物ではアルコールに近い挙動を示すが、それ以下では官能基を持たない炭化水素化合物の蒸発潜熱より、さらに小さくなる。
カルボン酸の異常について沸点と蒸発潜熱のどちらがおかしいのか見ておこう。
カルボン酸の分子量に対して沸点をプロットすると下図のようになる。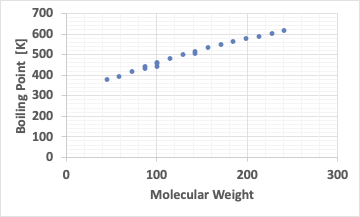
特に異常はない。
分子量に対して蒸発潜熱をプロットすると下図のようになる。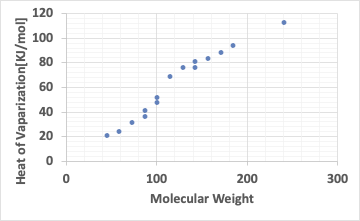
分子量が100を超えるあたりで断絶がある。
この現象は、化学工学で蒸留を扱う分野ではよく知られた現象である。
一般的には、炭素数が4以下のカルボン酸では下のような水素結合でダイマーを作って蒸発すると蒸留分野では信じられている。(気相のIRで、ダイマーで飛び回っているのが確認されている。)
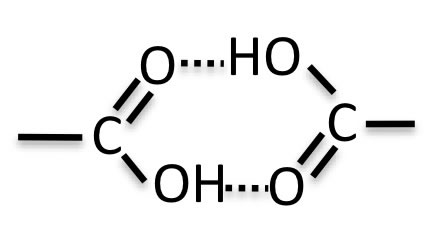
Drag=回転, Drag+Shift キー=拡大、縮小, Drag+コマンドキーかAltキー=移動。
Drag=回転, Drag+Shift キー=拡大、縮小, Drag+コマンドキーかAltキー=移動。
そこで、いろいろな種類の化合物で同じぐらいの沸点を持つ化合物をデータベースから抜き出し、検証してみた。下の図に示す化合物はほぼ同じような沸点を持つ。その化合物の温度に対する蒸発潜熱の値をプロットしてみると、やはり、isobutyric acidだけ異常値をとっているとしか思えない。
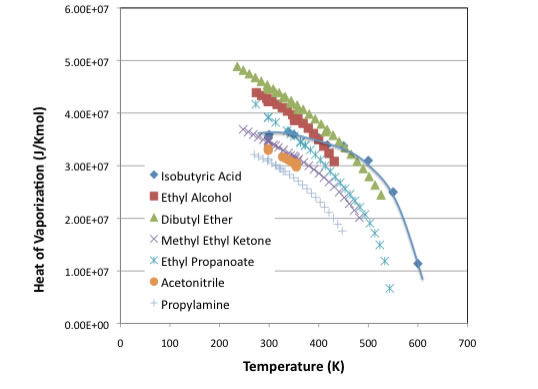
こうした結果が得られると、dHをドナー・アクセプターに分割して評価しなくては駄目だとかいう誘惑に駆られる。しかし、話はそんなに単純ではない。さらに検討が必要な項目だ。
話はもどるが、それでは、何故HPLCシミュレーションがうまく言ったのだろうか? これはおそらく、このHPLCの測定は 0.1% のリン酸バッファー(H3PO4/aq)を使っているので、ダイマーはいないのであろう。
解析例トップ
HSP基礎トップページ
分析関係トップページ
Copyright pirika.com since 1999-
Mail: yamahiroXpirika.com (Xを@に置き換えてください)
メールの件名は[pirika]で始めてください
