2022.9.10改訂(2021.2.2、2010.3.3)
解析例トップ >
医薬品・化粧品トップページ >
その他トップページ >
HSP基礎トップページ >
概要
顔料などの無機物をHSPで扱う時の基本的な方法をTiO2系顔料で説明する。
顔料は溶媒中に入れても溶解もしないし、膨潤もしない。
そのような時には、例えば懸濁安定性で溶媒を2つのカテゴリーに分け、Sphereプログラムを使いHSPを決定する。
表面修飾のやり方によってHSPがどう変化し、懸濁安定性がどうなるか理解しよう。
内容
酸化チタンの表面修飾に関する非常におもしろい論文があった。
色材協 67[8], 489-495 (1994)
資生堂の研究者の論文で表面修飾したTiO2を様々な溶媒にいれ、その分散安定性からハンセンの溶解度パラメータ(HSP)を決めていた。
古い論文なのでHSPを決めるのにTeas Plot(三角図)を使っている。
そこで、最新のやり方なら、こうした無機物のHSPがどのように求まるのか、例題として解析してみる。
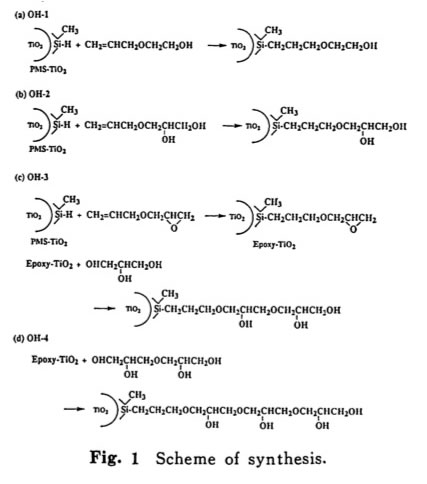
彼らの論文中では、上記のスキームに従ってTiO2の表面を修飾した固体(M-TiO2)を得ている。
そしてそのM-TiO2を様々な溶媒中にいれ、分散安定性を評価している。
分散安定性文献データ
評価は次の指標で行っている。
1: 30分以内に沈殿し上澄み液は透明になる。
2: 4時間経っても一部懸濁している。
3: 24時間経っても一部懸濁している。
4: 24時間以上懸濁している。
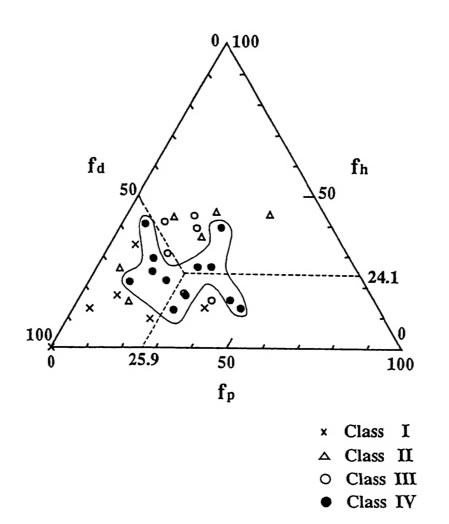
そしてTeas Plot(三角図)を使って、各TiO2のHSPを決定している。
| dD | dP | dH | Ra | |
| original-TiO2 | 17.02 | 9.2 | 13.2 | 4.87 |
| OH-1 | 17.02 | 9.2 | 11 | 4.08 |
| OH-2 | 16.92 | 11.8 | 12.2 | 4.62 |
| OH-3 | 16.28 | 8.2 | 10.8 | 3.62 |
| OH-4 | 16.38 | 7.4 | 12.4 | 2.85 |
実験的に無機物分散体のHSPを求めるのは、この方法をとる事が多い。
ただし、上のTeas Plotを見ても分かるように、クラスIVの溶媒を囲む領域は非常に複雑な形になり、これからHSPを決めるのはとても難しい事になる。
現在の標準法は、HSPの値をベクトルに見立てて3次元空間にプロットし、Sphere(球)を求めて解析をするHansen先生のやり方です。
このSphereモデルでは、良く分散する溶媒のベクトルがすべて球の内側に入り、それ以外のものが球の外に来るような、最小半径の球を求める。(もちろん例外は発生するが。)
そしてその球の中心をM-TiO2のHSPとする。
ここではクラスIVの溶媒をScore=1(良く分散する)それ以外の溶媒をScore=0(分散しない)と定め、Sphereを決定した。結果を下のテーブルに示す。
| dD | dP | dH | Ra | exceptions | |
| original-TiO2 | 15.14 | 15.16 | 5.18 | 9.65 | 6 |
| OH-1 | 15.24 | 6.13 | 16.77 | 6.55 | 1 |
| OH-2 | 15.95 | 7.10 | 17.14 | 7.45 | 2 |
| OH-3 | 15.42 | 9.08 | 13.45 | 6.04 | 2 |
| OH-4 | 15.18 | 8.87 | 15.03 | 5.32 | 2 |
もとの論文では、オリジナルのTiO2のdHが13.2で最大となっている。
これは考えてみると不思議だ。
TiO2の表面をOH基で修飾したらdH(水素結合項)が値が小さくなると言っている。
私の結果ではオリジナルのTiO2のdHは5.18で、修飾するにつれdH値が大きくなった。
dHが一番大きくなるのはOH-2の時だ。
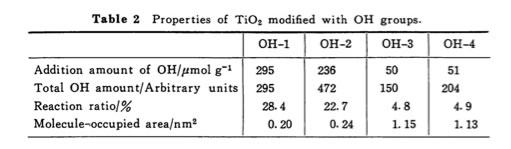
これは表面修飾の量が下のテーブルに示すように、側鎖が長くなるにつれ減ることに起因するのだと思う。
2011.4.22
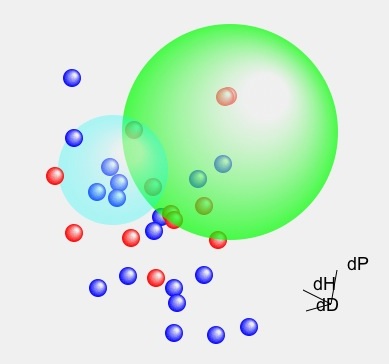
この時の3次元の位置関係を実際に見てみよう。
緑の球は私が計算した物、水色の球は論文に記載の球を示してある。
Original-TiO2
OH-1
OH-2
OH-3
OH-4
Drag=回転, Drag+Shift キー=拡大、縮小, Drag+コマンドキーかAltキー=移動。
溶媒をクリックすれば溶媒の名前が現れる。
Sphere が見えない場合(▶︎をクリックして開く)
 original TiO2
original TiO2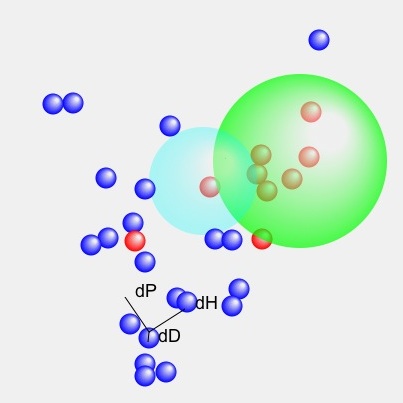 OH1
OH1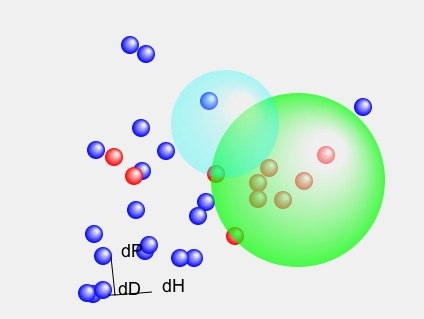 OH2
OH2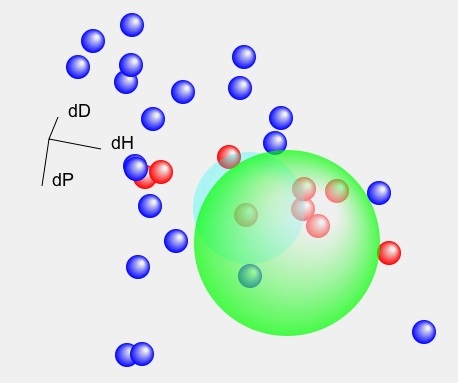 OH3
OH3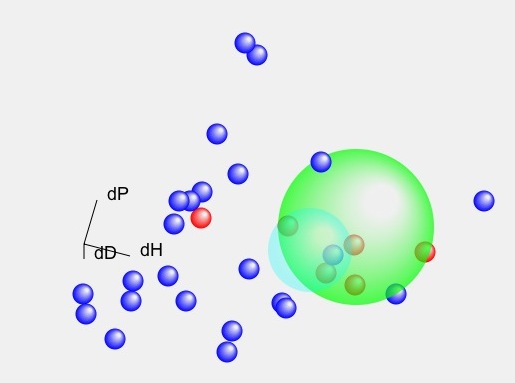 OH4
OH4
このSphereモデルは非常に単純で、ある任意の溶媒の分散性が知りたければ、HSPベクトルが球の内側であれば良く分散する、球の外側であれば分散しない,球の表面であれば微妙と判断できる。
この場合はM-TiO2では2個程度の例外が現れる。
OH-1の場合、 Cyclohexanoneが例外となる。
HSP距離を半径で割った値は1.99と大きく外れるのに、良く分散する。
OH-2, OH-3の場合は CyclohexanoneとAcetophenoneが例外になる。
OH-4の場合は, Cyclohexanoneと Ethylcellosolveが例外になります。
何故、 Cyclohexanoneは例外になるのだろうか?
この CyclohexanoneはオリジナルのTiO2に対しては良分散の溶媒だ。
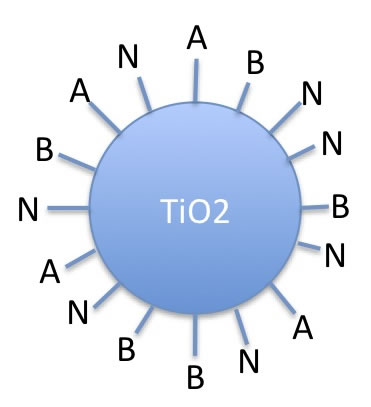
そこで、この現象は次のように考える事ができる。
オリジナルのTiO2の表面にはいくつかの異なった性質の表面が存在するのだろう。
オーバーオールのHSPは[15.14, 15.16, 5.18]になるが、表面の部分部分は異なったHSPを持つと考えられる。
そこで、オリジナルのTiO2は多くの例外(6個)を持つ。
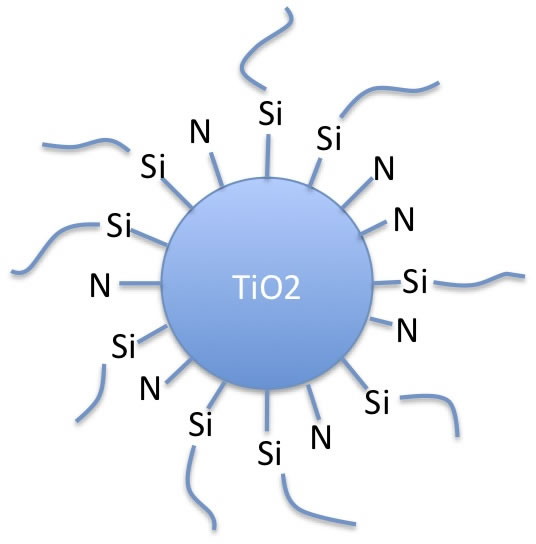
表面に1−2個水酸基を入れたものは、部分部分すべてが反応してしまうのでは無く、一部反応していない表面が残っているのだろう。
模式図で言えばNの部分は残る。このNの部分のHSPが CyclohexanoneのHSPに非常に近いと考えられる。
そこでM-TiO2のHSPに近いものと、 Cyclohexanoneに近いものは分散できることになる。
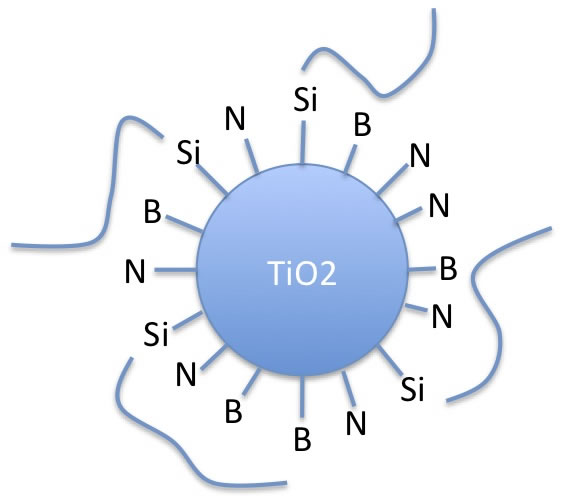
OH-3, OH-4のものは、やはりNの部分が残るので Cyclohexanoneには分散する。
ただし、修飾基が長くなった分、保護コロイド的に表面を覆うため、反応は進まなくなり、OHの導入量は上がらなくなるのだろう。
また、Sphereの半径も短くなる。
(良溶媒が少なくなる)
無機物や(ポリマーもそうかもしれないが)固体表面に様々な領域がある物質の分散/溶解を考えるのは大変な事ではあるが、HSPを正しく使うとずいぶんとすっきりと分かったような気にさせてくれる。
このM-TiO2は化粧用に使われるものだと思うが、次にはこうした修飾された表面と皮膚との相互作用を考えなくてはならない。
もし皮膚のHSPについて知りたければ、HSPiPを購入してe-Bookを読んで欲しい。
こうした解析法は、塗料用の顔料の表面修飾などにも使える非常に応用範囲の広い技術であるので是非活用して欲しい。
顔料の分散性は水素結合項を酸性/塩基性に分割する方法も有効です。
解析例トップ >
医薬品・化粧品トップページ >
その他トップページ >
HSP基礎トップページ >
Copyright pirika.com since 1999-
Mail: yamahiroXpirika.com (Xを@に置き換えてください)
メールの件名は[pirika]で始めてください
