

| ホームページ | Pirikaで化学 | ブログ | 業務リスト | お問い合わせ |
| Pirikaで化学トップ | 情報化学+教育 | HSP | 化学全般 |
| 情報化学+教育トップ | 情報化学 | MAGICIAN | MOOC | プログラミング |
2012.9.16
出光興産、三菱石油、日本石油、コスモ石油
化学工学のベースは、石油化学がほとんどすべてでしょう。
が、日本は石油の産出はありません。
最近、アメリカなどで”シェールガス革命”とかにぎわっていますが、このシェール類も日本は算出しません。
と思っていたら山形のあたりで見つかったとの報道も飛び込んできました。
(2012.10.3 初めてのシェールオイルが秋田で出てきたとニュースにありました。地下1800m, シェール層を酸性の液体で溶かし窒素の圧力で回収したとありますがが、そんなことして環境破壊はどうするのでしょうか?)
シェールガスは主成分はメタンで、石油と違って蒸留もいらないので化学工学の授業のネタ的には面白くありません。
シェールオイルまで含めると少しは授業に使えそうなので見てみましょう。
シェールガスについてはWikiPediaを参照してください。
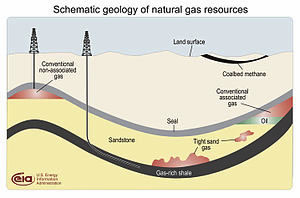
シェールガスの賦存(黒色部分)。
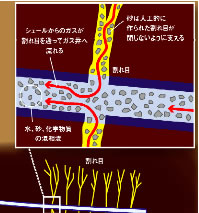
シェールガスを含む頁岩層(Gas-rich shale)に水平にパイプを入れ、高水圧で人工的に割れ目をつくり、ガスを採取します。
この圧入される水には、さまざまな化学品が添加されます。
などが液体全体の 0.5 % 程度、圧入水に添加されています。
0.5%といっても、入れる水の量も半端でないので、環境汚染が非常に問題になっています。
これらのうちイソプロピルアルコール、エチレングリコール、ホルムアミド、グルタルアルデヒドについて、2011年講義資料のやり方で環境影響評価してみましょう。
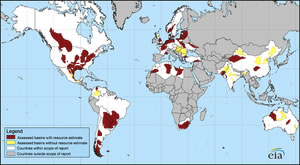
シェールガスはいろいろな所に分布します。
オイルシェールについても、WikiPediaの記事を参照してください。
自分の理解した範囲では、石油、石炭、天然ガスのように簡単に採取できるものでは無いが、広く、薄く、大量に存在している炭化水素化合物が採取可能になったということらしいです。
こうした、石油になりそこなった炭化水素を扱うには、熱分解して合成石油にして用いたりしています。
シェールガスについては非常に良くまとまった資料がJOGMECから出ています。
それでは、石油、石炭、シェール類、まとめて分子レベルで理解してみましょう。
メタン(CH4)は天然ガス、シェールガスの主成分で一番小さな炭化水素です。
天然ガスにはメタン・エタン・プロパン・ブタン・ペンタン以上の炭素化合物や窒素が含まれ、産出する場所によってその割合は少しずつ異なります。
産地による成分の違いの例(WikiPedia)(単位は mol/100mol)
産地 メタン エタン プロパン ブタン ペンタン 窒素
ケナイ(アラスカ) 99.81 0.07 0.00 0.00 0.00 0.12
ルムート(ブルネイ) 89.83 5.89 2.92 1.30 0.04 0.02
ダス(アブダビ) 82.07 15.86 1.86 0.13 0.00 0.05
メタンからプロパンまでは異性体は存在しません。
炭素が4つになった、ブタンからは異性体が存在します。
ブタンを目にするのは、ライターやボンベ式の調理器具でしょう。
圧力をかけると液化し、圧力がなくなれば簡単に気化するので、それに火花で着火して用います。
炭素数が増えるにつれ、異性体の数は指数関数的に増えていきます。
C4H10 2種類
C5H12 3種類
C6H14 5種類
C7H16 9種類
C8H18 18種類
C9H20 34種類
C10H22 77種類
鎖状のアルカン化合物でこれだけありますが、同じ炭素数でも環状、アルケン、アルキン化合物まで含めると膨大な数の化合物を扱わなくてはなりません。
C8の化合物で一般的に目にするのは、ガソリンの主成分、イソオクタンでしょう。
普通イソオクタンと言った時には2-メチルヘプタンなのですが、石油関連では、2,2,4-トリメチルペンタンをイソオクタンと呼びます。
現実的には単品はあり得ず、例えば高純度ヘキサンをガスクロに打てば20本以上のピークが現れます。
沸点が近い化合物が様々に混じったものが現実の製品になります。
C8H18では最大でも沸点は125℃、C9H20で151℃、C10H22で174℃です。
従ってオイルシェールの中にはC8H18以下の分子量の化合物はほとんど居ない事が下の資料からわかる。
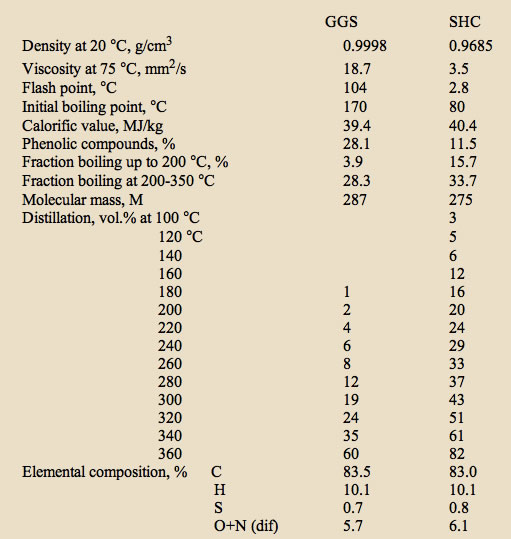
こうした高沸点成分は熱分解して合成石油として利用されます。
そこで今回の解析はC8成分以下に限り考えてみましょう。
C8以下データ
炭素数が8のオクタン類、鎖状のものだけで、18種類ありますが、その分子式はC8H18で皆共通です。
しかし、沸点はn-Octaneの398.83Kから、2,2,4-trimethylpentaneの372.39Kと26℃異なります。
この沸点の推算に関して、YMBはC3からC8で下のグラフに示すように精度高く沸点を推算する事ができています。
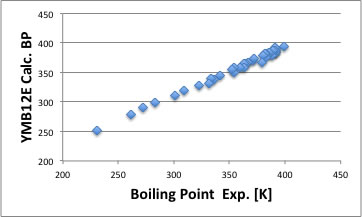
どうして、分子式C8H18と共通なのに、沸点の推算結果が変わるのでしょうか?
それはYMBでの分子の分割方法が、大きな原子団から認識していくのでこのような結果になります。
原子団がCH3, CH2, CH, Cしか定義されていなければ、t-ButylはCH33個、C1個ですが、C4の原子団まで定義されているYMBではt-Butylとして認識されます。
このように原子団の定義を増やせば増やすほど精度はあがりますが、物性推算式を構築するために必要なデータ数は飛躍的に大きくなります。
それでは、C3からC8まで分子のSmilesの構造式を、YMBを使って計算し、テーブルにまとめましょう。
これらの化合物で全く同じ原子団の組になってしまう化合物があるか確認しましょう。
原子団寄与法は非常に簡便な方法ですが、実は致命的な欠陥もあります。
例えばアクリル酸メチル(CH2=CHCOOCH3)と酢酸ビニル(CH2=CHOOCCH3)はエステルのつく向きが逆なだけで、原子団的には、CH2=, CH=, COO, CH3と全く同じになってしまい、全ての物性計算結果は同じになります。
ここでは、コンピュータの利用が進む、ずーっと以前から知られていた炭化水素の異性体の取り扱いを学んでおきましょう。
それは球形の分子は棒状の分子よりも沸点が低いというトポロジカルな原理に基づいています。
同じ体積(例えば同じC8H18)なら球は最も表面積が小さくなります。
分子同士の相互作用は接触面積の大きさに比例するとしますと球形の分子の沸点は一番小さくなります。
では、コンピュータを使って3次元構造から分子表面積を計算できなかった時代、どのようにしてこの問題を取り扱ったのでしょうか?
一番簡便な方法はMCI(Molecular Connectivity Index)を使うやり方でしょう。このMCIは分子中の全ての原子に対して、何個の重原子と結合しているかを数え上げます。
例えば3-Methyl Pentaneでは下図(I)のようになります。
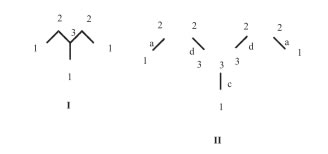
次に分子を分解し、各結合の両端が何個(δi, δj)の重原子に結合しているか、上図の(II) を作ります。
そして、(δi * δj)-0.5 を各結合について計算し総和を取ったものがMCIになります。

このMCIの値は枝分かれ構造が多くなるにつれ小さな値になることが上のテーブル(右の列がMCIの値)から分かります。
このMCIの興味深い点は、例えばC7H16になった場合、n-heptaneのMCIはHexaneより結合が一つ増えた分、MCI=3.414と大きくなります。
C7H16で最も枝分かれが大きくMCIが小さくなるのは、2,2,3-trimethylbutaneで, MCI=2.943です。
これはMCI的にはn-hexaneに非常に近い。このように分子をMCIで見た場合に、非常に良好な連続性が得られる事が知られています。
例えばC3-C8の化合物の沸点を分子量に対してプロットすると下のようになります。
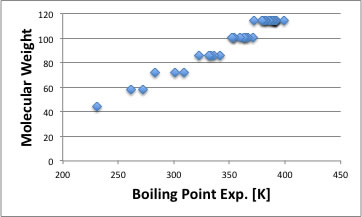
異性体は分子量が変わらず、沸点は異なるのでこのような結果になります。
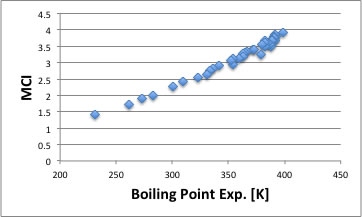
これをMCIに対してプロットすると非常に良好な直線が得られます。
この事は、炭素の数が増減する事による沸点の変化と球状に近づく事による沸点の変化を、MCIは連続的に等価に扱える事を示しています。
こうしたシェール類の物性で一番重要なのは沸点でしょう。
シェール類は地下に高圧水を注入して頁岩を破砕しながら回収します。
そうした炭化水素が水にどれだけ溶けるかは重要な指標でしょう。
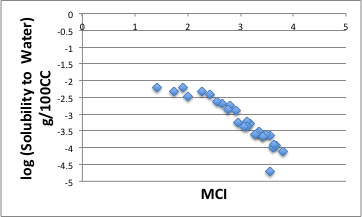
log(水への溶解度)は下図に示すようにMCIと非常にきれいな相関があります。 (プロットは実験値に対するものであるが、 YMB計算値に対してプロットしてみよう。)
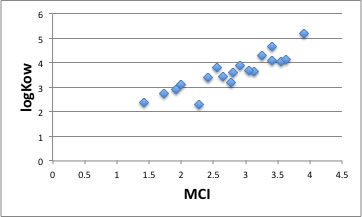
オクタノール/水分配比率, logKow(logP)の値もMCIときれいな相関があります。
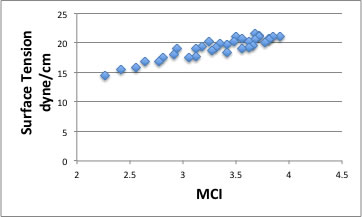
表面張力とMCIの相関。
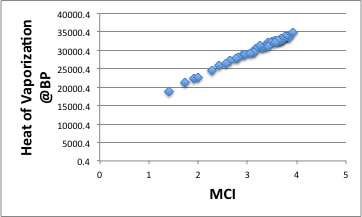
沸点に於ける蒸発潜熱もMCIと相関があります。
引火点とMCIの相関。
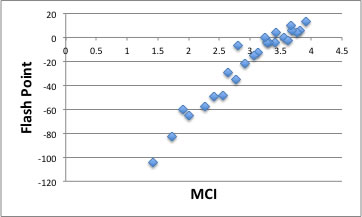
異性体を扱う上で、MCIは非常に役に立つ指標だったのですが、コンピュータの発展とともに失われてきています。
トポロジーはコンピュータの弱い分野だったのでしょう。
ついでにオクタン価について見てみます。
ガソリンエンジンは、火花で着火して燃料を燃焼させます。
そして、燃料の未燃焼部分が自然発火すると、ノッキングという現象がおこります。
燃料の自然発火のしにくさは「オクタン価」で表されます。
オクタン価とは自然発火しにくいイソオクタン(2,2,4-トリメチルペンタン)のオクタン価を100とし、自然発火しやすいn-へプタンのオクタン価を0として値を決めたものです。
化学便覧の中に次のようなグラフがあります。
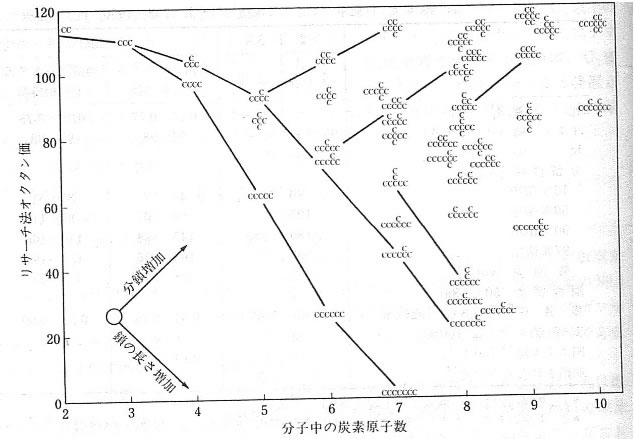
炭素数が大きくなるに連れオクタン価は下がり、同じ炭素数なら枝分かれが多くなるとオクタン価は高くなります。(オクタン価の値は細矢先生の資料がこちらにあるので参照してください)
細矢先生の本が出版されました。
「トポロジカル・インデックス」フィボナッチ数からピタゴラスの3角形までまでをつなぐ新しい数学,
日本評論社
「はじめての構造化学」構造化学のなぜに答える。
オーム社
是非一読をお勧めします。
ガソリンは自然発火がおこりにくい方が性能が高くなります。
一方、ディーゼルエンジンの燃料は多様なものが使用できますが、一般的には軽油や重油が使われます。
軽油は主要成分が200-350℃での沸点を持つのに対して、ガソリンエンジンで使用されるガソリンは30-220℃程度の沸点を持ちます。
このことがガソリンを揮発しやすく危険なものにしています。
また、この2つ燃料の引火点についても軽油の方がガソリンより高く、逆に発火点は沸点や引火点と異なり、軽油の方がガソリンより低くなります。
この両者の特性から、ガソリンは火に近づけるだけで危険なのに、軽油に火を近づけてもすぐには燃えません。
火が無い環境でこれら2つの温度を上げてゆくと先に自ら火が着くのは軽油であり、この軽油の発火点の低さがディーゼルエンジンでの使用を容易にしています(WikiPedia)。
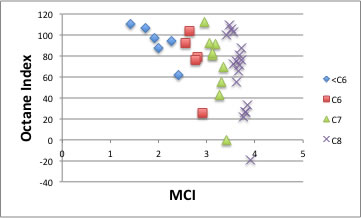
このオクタン価をMCIに対してプロットすると、同じ炭素数に対しては傾向が出ますが、炭素数の違いまでは吸収できないようです。
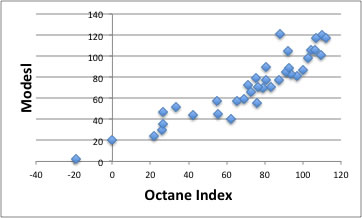
YMBを使い各分子を計算し、MCI以外どの変数を選択すればモデルが構築できるか考えてみましょう。
各化合物の自然発火温度(AIT)の値も先のテーブルに記載してある。発火温度のモデル式を作ってみましょう。
石炭は石炭で、どう利用して行くか考えなくてはならないでしょう。
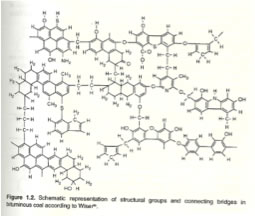
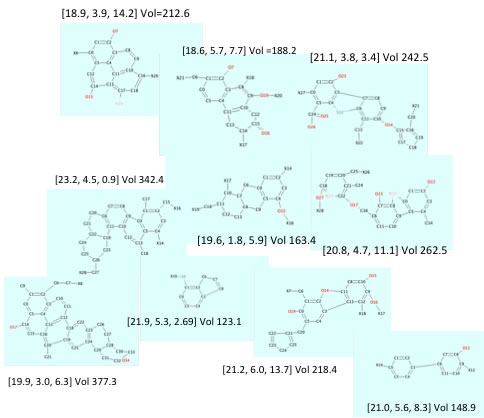
領域ごとにハンセンの溶解度パラメータ(HSP)が計算されて、溶解度が検討されています。
それに関してはこちらを参照してください。
シェールガス革命となると実は困ってしまうのがブタジエンを原料に使っているゴム産業です。
2011年講義資料のブタジエンの抽出蒸留を参照してください。
自由研究
このMCIは鎖状の飽和炭化水素で構築された技術です。
従って、CH2=CHCH3とCH3CH2CH3では同じ値になってしまいます。
不飽和の炭素、環状の炭素のMCIの補正係数を決定してみましょう。
具体的にはオレフィン化合物(環状化合物)の沸点が、鎖状の飽和炭化水素のMCIと沸点の直線に乗るように補正係数を定めます。
Copyright pirika.com since 1999-
Mail: yamahiroXpirika.com (Xを@に置き換えてください) メールの件名は[pirika]で始めてください。