Заметка №1
10 веских причин, почему следует использовать параметры растворимости Хансена (HSP)
18.08.2009
Существует множество теорий растворимости: MOSCED, UNIFAC, Jouyban-Acree, Yalkowsy, MOD (Mobile Order and Disorder). Все они по-своему привлекательны.
Также мы с большим уважением относимся к пионерским работам профессора Гильдебранда в области изучения параметров растворимости (ПР). Без работ Гильдебранда параметры растворимости Хансена просто не существовали бы. Но на данный момент мы готовы представить 10 веских причин, почему следует использовать HSP, а не другие теории. (В статье используются особенности версии 3, которых нет в версиях 1, 2, 2+).
- Параметры растворимости Хансена (HSP) включают в себя параметр растворимости Гильбранда
Параметр растворимости Гильдебранда можно рассчитать, зная параметры растворимости Хансена по соотношению:
(ПР Гильдебранда)2 = ∑HSP2 = dD2 + dP2 + dH2
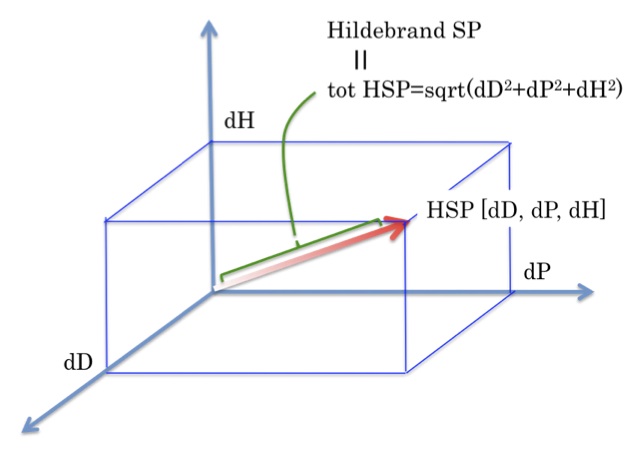
Если вы настаиваете на использовании ПР Гильдебранда, можете просто воспользоваться ∑HSP2.
В том случае, если параметры растворимости Хансена (HSP) изображают в трехмерной системе координат как точку HSP с координатами (X, Y, Z) = (dD, dP, dH), то параметр растворимости Гильдебранда будет равен длине радиус-вектора этой точки HSP. Таким образом, параметры растворимости Хансена(HSP) полностью включают себя параметр растворимости Гильдебранда.
Что же говорит нам параметр растворимости Гильдебранда, когда длины радиус-векторов для различных соединений совпадают? Будут ли эти соединения иметь одинаковую растворимость? Мы отобрали 391 соединение, для которых параметр растворимости Гильдебранда одинаков и равен 19±0,3, и построили трехмерный график:
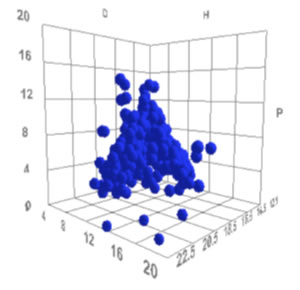
Некоторые соединения характеризуются большой составляющей дисперсионного взаимодействия dD и малыми составляющими полярного dP и взаимодействия водородных связей dH; некоторые большими dD и d H; другие – большим dP.
Но длины радиус-векторов (расстояние от точки начала координат [0,0,0]) почти одинаковы для всех и равны 19,0.
С точки зрения параметров растворимости Хансена эти соединения имеют различную растворимость. Когда мы говорим «подобное растворяется в подобном», под «подобным» мы подразумеваем «близкое к точке HSP», не к длине радиус-вектора этой точки.
2 Теория HSP имеет понятие радиуса взаимодействия.
(статьи по теме: статья1, статья2)
Используя «справочник полимеров», можно найти информацию о растворимости или нерастворимости того или иного соединения. Например, растворители поливинилхлорида (ПВХ) заносим в таблицу с цифрой 1, а вещества, не растворяющие ПВХ – с цифрой 0.
Название |
dD |
dP |
dH |
Растворитель/ |
tem |
Объем |
Хлорбензол |
19 |
4.3 |
2 |
1 |
|
102.1 |
Циклогексанон |
17.8 |
8.4 |
5.1 |
1 |
104.2 |
|
Циклопентанон |
17.9 |
11.9 |
5.2 |
1 |
89.1 |
|
ДМФА |
17.4 |
13.7 |
11.3 |
1 |
77.4 |
|
ДМСО |
18.4 |
16.4 |
10.2 |
1 |
71.3 |
|
Метилэтилкетон |
16 |
9 |
5.1 |
1 |
90.2 |
|
Нитробензол |
20 |
10.6 |
3.1 |
1 |
102.7 |
|
ТГФ |
16.8 |
5.7 |
8 |
1 |
81.9 |
|
1,2-дихлорбензол |
19.2 |
6.3 |
3.3 |
1 |
113 |
|
Диизопропилкетон |
15.6 |
6.7 |
4.1 |
1 |
140.2 |
|
Диоксан |
17.5 |
1.8 |
9 |
1 |
85.7 |
|
Этиленхлорид |
18 |
7.4 |
4.1 |
1 |
79.4 |
|
Изофорон |
17 |
8 |
5 |
1 |
150.3 |
|
Мезитилоксид |
16.4 |
7.2 |
5 |
1 |
115.2 |
|
Толуол |
18 |
1.4 |
2 |
1 |
106.6 |
|
Ацетон(SW) |
15.5 |
10.4 |
7 |
0 |
73.8 |
|
Ацетангидрид(SW) |
16 |
11.7 |
10.2 |
0 |
95 |
|
EtOH |
15.8 |
8.8 |
19.4 |
0 |
58.6 |
|
Анилин(SW) |
20.1 |
5.8 |
11.2 |
0 |
91.6 |
|
Сероуглерод |
20.2 |
5.8 |
0.6 |
0 |
60.6 |
|
Уксусная кислота |
14.5 |
8 |
13.5 |
0 |
57.6 |
|
Этилацетат |
15.8 |
5.3 |
7.2 |
0 |
98.6 |
|
Гексан |
14.9 |
0 |
0 |
0 |
131.4 |
|
Винилхлорид |
16 |
6.5 |
2.4 |
0 |
|
64.7 |
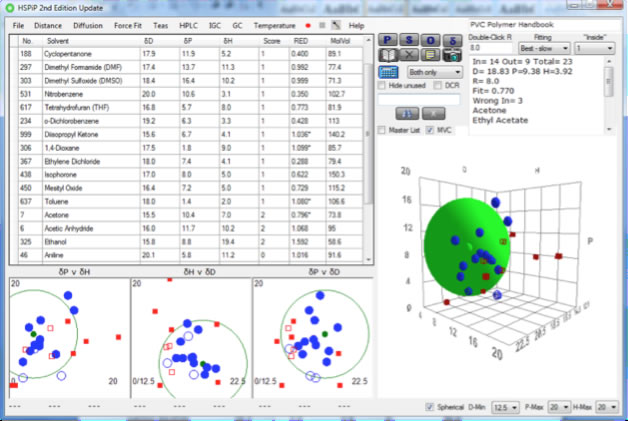
Используя эти данные, можно с большой точностью рассчитать параметры растворимости Хансена (HSP) для ПВХ:
12.04.2011
Если вы используете браузер, поддерживающий HTML5: например, Chrome, Safari или FireFox4 (с IE9 возникают проблемы), то можете увидеть эту область: 2 области, 1 область. (перетащите рисунок, чтобы повернуть его; перемещение рисунка с нажатой клавишей Shift позволит приблизить/удалить изображение, перемещение с нажатой клавишей Alt (доступно только для Мас) - перевод). Если нажать на растворитель (маленький шарик), появится название.
Хорошие растворители обозначены синим цветом, плохие – красным, в центре области - наилучший растворитель для ПВХ. Граница области отделяет хорошие растворители от плохих. Зная интервал параметров растворимости HSP для каждого растворителя (Ra), можно определить относительную разность энергий (RED) RED=Ra/R0, и неважно, находится ли растворитель внутри области или вне ее.
Если RED < 1, молекулы подобны и будут растворяться;
Если RED = 1, система частично растворима;
Если RED > 1, система не растворима.
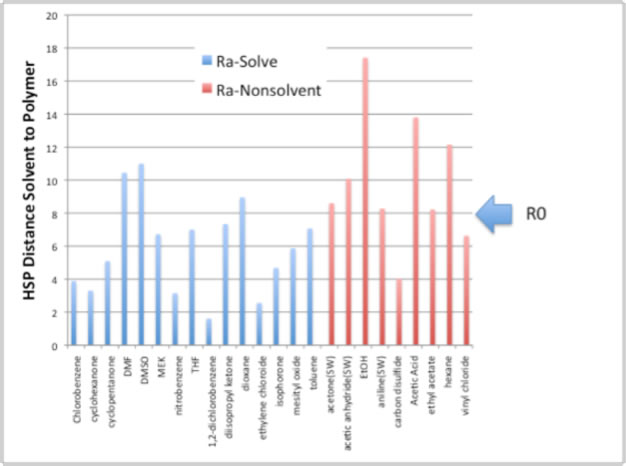
Если Ra > 8, растворители не будут растворять ПВХ. ДМФА, ДМСО и диоксан – исключения. Если Ra < 8, растворители будут растворять полимер, кроме сероуглерода и винилхлорида. Существует ряд причин, когда при Ra<R0 соединение не будет растворять полимер. Иногда молекулярные объемы растворителя настолько велики, что они просто не могут проникнуть в полимер. Также параметры растворимости Хансена – не кинетические показатели, поэтому невозможно предсказать, сколько потребуется времени на растворение полимера.
Существуют исключения, но с практической точки зрения, знание HSP помогает исследователям подобрать хорошие растворители.
Анализ растворимости полимера с учетом параметра растворимости Гильдебранда показывает, что результаты неверны.
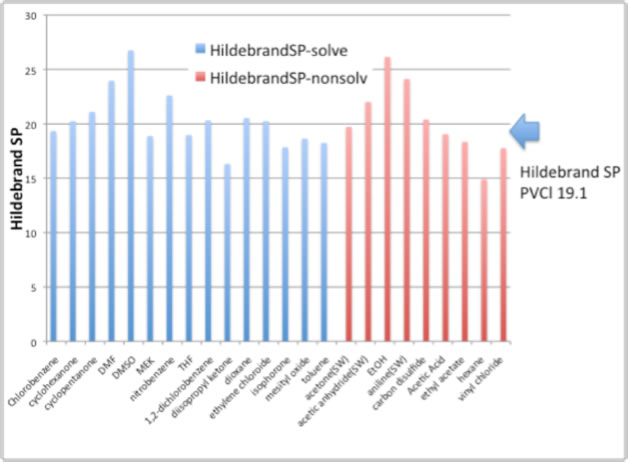
В этом случае мы никак не может определить, будет ли растворитель растворять ПВХ.
К сожалению, остальные теории растворимости не позволяют определить области растворимости, Ra, RED и т.д., и поэтому не представляют практического интереса для реальных ученых.
3 HSP подходить для многокомпонентных систем
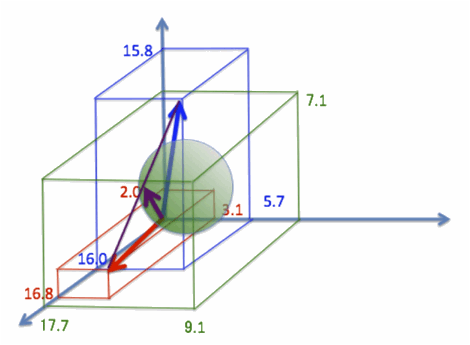
Смеси растворителей представляют трудности для изучения для других теорий растворимости. В HSP смесь растворителей учитывается простым «сложением радиус-векторов». Существует множество примеров, когда два «нерастворителя» в смеси образуют хороший растворитель. Например, ПММА [17.7, 9.1, 7.1] (зеленый) нерастворим в бутаноле [16.0, 5.7,15.8] (синий) и диэтилсульфиде [16.8, 3.1, 2.0] (красный). Вы видите, что синий и красный векторы расположены довольно далеко от центра зеленой сферы. Но смесь бутанола и диэтилсульфида в соотношении 50:50 при сложении с учетом концентраций дает новый вектор – фиолетовый [16.4, 4.4, 8.8], который очень близок к центру зеленой сферы, и вот эта смесь уже растворяет ПММА!
12.04.2011
Если вы используете браузер, поддерживающий HTML5: например, Chrome, Safari или FireFox4 (с IE9 возникают проблемы), то можете увидеть эту область. (перетащите рисунок, чтобы повернуть его; перемещение рисунка с нажатой клавишей Shift позволит приблизить/удалить изображение, перемещение с нажатой клавишей Alt (доступно только для Мас) - перевод). При нажатии на растворитель, появится название.
Это явилось одним из первых доказательств теории HSP, а также весьма весомым доводом в пользу использования именно этой теории. Сейчас же можно говорить еще об одной причине, почему следует использовать HSP для бинарных систем: в новой версии HSPiP доступны коэффициенты активности, константы Генри, параметр Маргулиса и азеотропные системы.
4 HSP подходит для определения растворимости нерастворимых веществ
(статьи по теме: статья1, статья2)
В основном, параметр растворимости определяется теплотой парообразования. Поэтому для химических веществ, которые не испаряются, нет прямого пути определения параметра растворимости. Например, ионные жидкости имеют низкое давление насыщенных паров и, как следствие, для них нельзя найти параметр растворимости через теплоту парообразования. Но мы можем определить HSP, пользуясь методикой, описанной в разделе 2. Также можно определить HSP для наноуглерода, пигментов, стекла. Существуют некоторые возражения, что и параметр растворимости Гильдебранда можно использовать для определения растворимости нерастворимых (неиспаряемых) веществ. Например, была измерена растворимость С60 в нескольких растворителях.
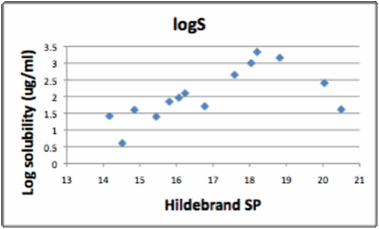
Кажется, параметр растворимости Гильдебранда для С60 имеет хорошую корреляцию, и автор статьи сделал вывод, что параметр растворимости Гильдебранда для С60 равен 18,4. Но несколько лет спустя, были опубликованы другие данные. Когда мы нанесли все данные на график, то увидели, что все точки разупорядочены.
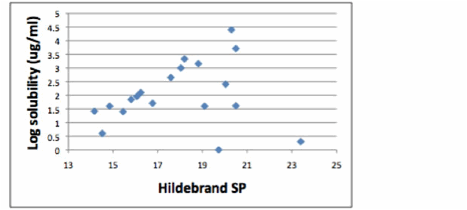
Самая верхняя точка соответствует 20,3 (25000 мг/мл), но рядом находится точка, соответствующая растворителю с параметром растворимости Гильдебранда = 19,7, способному растворить всего 1 мг/мл. Таким образом, для очень узкого диапазона растворителей параметр растворимости Гильдебранда хорошо согласуется, но в широком диапазоне растворителей все результаты оказываются спутанными (вы уже поняли причину, если прочитали раздел 1). Из экспериментов с областями растворимости мы определили, что HSP для С60 равен [20, 3, 2]. Сейчас мы можем нанести данные на график зависимости «удаленности от HSP С60» от «Log растворимости» для всех растворителей.
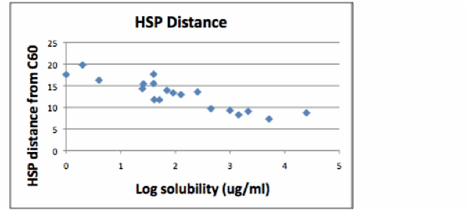
12.4.2011
Если вы используете браузер, поддерживающий HTML5: например, Chrome, Safari или FireFox4 (с IE9 возникают проблемы), то можете увидеть эту область. (перетащите рисунок, чтобы повернуть его; перемещение рисунка с нажатой клавишей Shift позволит приблизить/удалить изображение, перемещение с нажатой клавишей Alt (доступно только для Мас) - перевод). При нажатии на растворитель, появится название.
Наилучшим образом для этих данных подходит dD=22 вместо 20, но общая тенденция правильная.
Мы с легкостью можем объяснить зависимость «Короткое расстояние вектора = высокая растворимость».
Но необходимо прояснить одну деталь.
Когда мы говорим о длине вектора, мы имеем ввиду:
![]()
Обратите внимание! Перед dD стоит множитель 4.
Наличие множителя 4 сложно объяснить, но он необходим для HSP. Если вы хотите получить больше информации, пожалуйста, обратитесь к нашей книге «User’s Handbook» или электронной книге e-Book.
5 HSP имеет официальную базу данных
Мы имеем официальнуюбазу данных HSP для более чем 1200 химических соединений и 600 полимеров.
Кроме того имеется база данных, содержащая свыше 6000 расчетных параметров HSP. Сейчас мы накапливаем данные для новых соединений, используемых в парфюмерной промышленности, данные по бинарным системам и т.д., проверяя каждое значение одно за другим для обеспечения надежности наших вычислений. При составлении этих данных в других базах данных или справочниках обнаруживаются некоторые ошибки. Вот пример противоречивых данных для параметра растворимости Гильдербранда.
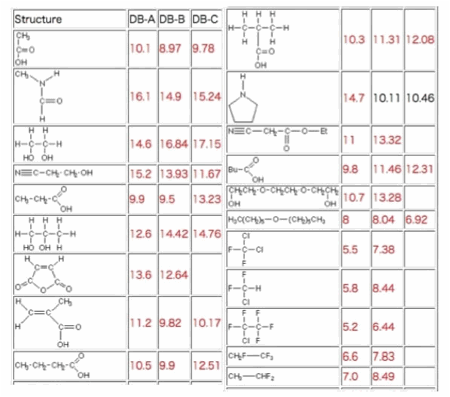
Значения DB-A, DB-B, DB-C из очень известных баз данных, и многие исследователи ими пользуются. Но значения параметра растворимости Гильдебранда ((кал/моль)^0,5) очень различны, особенно для карбоксильных и фторсодержащих соединений. Какое значение предпочесть? Параметр растворимости Гильдебранда удобен и широко используется, но нет официальных значений. Когда вы сталкиваетесь с подобной проблемой, возникает необходимость обращаться ко множеству литературных источников.
6 HSP имеет официальную литературу и официальное программное обеспечение «HSPiP»
HSP представлена в официальной литературе «Hansen Solubility Parameters A User’s Handbook» («Параметры растворимости Хансена. Справочник пользователя») и в электронной книге “HSPiP e-Book”, а также имеет официальное программное обеспечение.
Параметр растворимости Гильдебранда описан в многочисленных неофициальных литературных источниках, существует много программ расчета этого параметра, но как мы уже отмечали в разделе 5, для одних и тех же соединений представлены совершенно разные значения. Таким образом, расчетные значения напрямую зависят от источников данных, которыми пользуется исследователь. Вы не можете воспользоваться результатами другого исследователя, не зная, какой программой расчета, какой версией он пользовался. Мы день за днем разрабатываем литературу и программное обеспечение. Возможно, вы зададитесь вопросом, «покупать ли программу сейчас, а вдруг через некоторое время выйдет лучшая версия?». Но у вас есть причина купить сейчас, т.к. потребности клиента у нас в приоритете. Мы обновляем ПО в соответствии с пожеланиями клиента и на благо круга заинтересованных в HSP. Существующие пользователи имеет право бесплатного обновления, новые – вносят дополнительную плату за новую версию.
7 HSP применима для экспериментальных исследований
Можно ли заменить один растворитель другим только потому, что их растворяющая способность одинакова?
Параметры растворимости не говорят о самой растворимости. Но для экспериментов, например, температура кипения - очень важный параметр в процессе разработки новых растворителей для красок или чернил. Никому не захочется использовать краску, которой потребуется месяц, чтобы высохнуть, даже если используемый растворитель будет иметь ту же растворяющую способность, что и Уайт-Спирит, и не будет оказывать негативного влияния на окружающую среду и здоровье. Наше ПО HSPiP позволяет грамотно использовать растворители в своих экспериментальных исследованиях. Мы продолжаем обновлять программу, добавляя в нее различные функции по пожеланиям клиента.
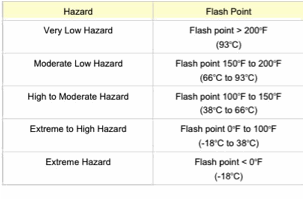
Наиболее важным параметром для растворителя является температура вспышки. Принадлежность к классу опасности определяется из диапазона температур вспышки. HSPiP позволяет определить не только растворимость, но и температуру вспышки, реакционную способность с гидроксильными радикалами, давление паров, коэффициенты распределения и др. Ни одна другая теория растворимости не имеет таких функций, и, как следствие, менее применима в практике.
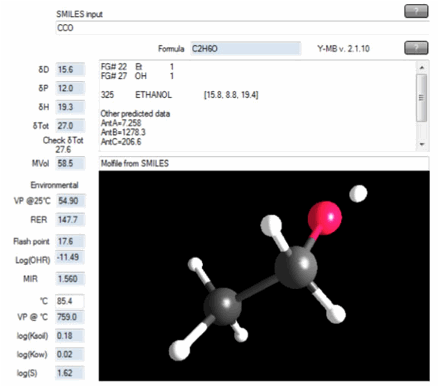
8 HSP взаимодействует с другими науками
(статьи по теме: статья)
HSP – это наука, а наука взаимодействует с другими науками, одной из которых является аналитическая химия, в частности, хроматография. Из данных изотермической газовой хроматографии можно рассчитать экспериментальные значения параметров растворимости HSP. А уже зная параметры растворимости, мы можем определить индекс удерживания вещества для газового хроматографа или время удерживания для ВЭЖХ (высокоэффективная жидкостная хроматография).
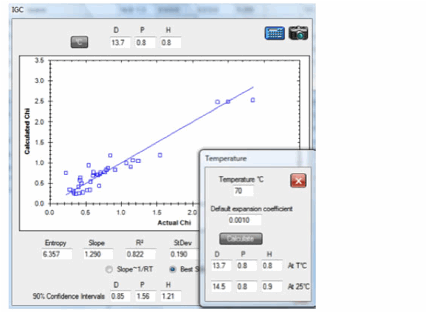
Мы также разрабатываем элементы взаимодействия с органическим синтезом, медициной, токсикологией, ветеринарологией, вкусовой и обонятельной областью.
9 Разнообразная теория HSP
Существует множество других теорий растворимости, но они используются небольшими группами в узких областях для конкретных целей. Только HSP применима в широком диапазоне задач. Ниже приведено содержание электронной книги. Вы и сами можете убедиться, насколько велика область применения HSP. Содержание электронной книги увеличивается с каждым изданием.
- Минимум теории. Почему HSP настолько «всесильна» и почему 3 числа имеют столь фундаментальное значение? Вы получаете минимум теории для максимального понимания.
- Сфера. Как понять теорию HSP в 3 значениях, используя мощное ПО Sphere, которое идет как часть комплекта.
- Как HSP поможет вас быстро найти подходящий растворитель для конкретных полимеров или красителей.
- Безопаснее, быстрее, дешевле. Используйте оптимизатор растворителей, чтобы найти более безопасную, быструю и дешевую смесь растворитель.
- Совмещение. Как HSP помогает совместить несмешиваемые полимеры.
- Адгезия. HSP лежит в основе экспериментальной адгезии.
- Оттенки черного. Как HSP может помочь в отношении непластичных материалов, таких как битумы, которым необходимо непосредственное взаимодействие с полимерами, чтобы стать пригодными для дорожных покрытий.
- Параметры «растворимости» нерастворимых веществ. Почему параметры «растворимости» широко применяются для нерастворимых веществ, таких как сажа.
- Трещины в системе. Как распознать тенденцию к долгосрочному разрушению вашего полимера от напряжений под влиянием окружающей среды.
- Внесем ясность. Использование HSP для разработки глянцевых покрытий.
- Набухание: в каком из растворителей будут набухать каучуки или полимеры.
- Использование HSP для понимания защитных свойств кожи и перчаток.
- HSP и диффузия. Мощная программа для моделирования процесса диффузии идет с пакетом, чтобы вы могли понять сложности абсорбции и десорбции растворителей и каким образом HSP способствует пониманию этих явлений.
- Спасение планеты. Использование HSP для решения множества экологических проблем.
- Уборка с использованием значений HSP и поверхностно-активных веществ. Впервые опубликован список значений HSP для широкого спектра поверхностно-активных веществ.
- Хроматография – создатель и пользователь HSP. HSP и хроматография включает программу для моделирования времени удержания ВЭЖХ и программу для моделирования изотермической газовой хроматографии.
- Ароматы искусственные и натуральные. HSP объясняет идею обнаружения запаха.
- Атакуя ДНК. Взгляд на цитотоксичность.
- Следуя за нано. Применение HSP к углеродным нанотрубкам, C60, наноклеям и квантовым точкам.
- Сделай сам. Способы расчета HSP для ваших молекул, включая все распространенные методы, плюс новый метод Стефаниса-Панайоту и автоматический метод Y-MB.
- Планы на будущее: книги и программное обеспечение.
10 HSP до сих пор разрабатывается при участии проф. Аббота, д-ра Ямамото и д-ра Хансена
Теория HSP – единственная теория, охватывающая широкий диапазон знаний и продолжающая интенсивно развиваться. В декабре прошлого года (2008 г.) мы выпустили первую версию программы, в марте (2009) – вторую, в июне – обновленную вторую, сейчас готовим третью версию. Мы улучшили программу, дополнили данные и добавили функциональность. Мы по-прежнему предоставляем клиентам то, что они хотят.