

| ホームページ | Pirikaで化学 | ブログ | 業務リスト | お問い合わせ |
| Pirikaで化学トップ | 情報化学+教育 | HSP | 化学全般 |
| 情報化学+教育トップ | 情報化学 | MAGICIAN | MOOC | プログラミング |
2012.1.12
三菱化学:p型有機半導体に、「テトラベンゾポルフィリン」と呼ばれる有機物を、n型有機半導体に、「フラーレン誘導体」を用いている。変換効率10%以上を達成。コスト従来の1/10。(太陽電池資料を参照の事)
ソニー:DuPont社のNafion膜と異なり、水分を必要としない。原料のメタノールが拡散してしてしまうことがないフラーレン膜。
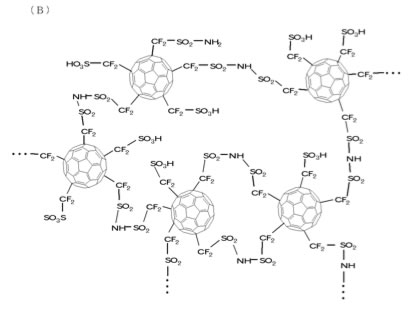 ソニー特許より
ソニー特許より
製造方法は、ベンゼン+空気+Arを燃焼させて煤を発生させる炭化水素燃焼法が三菱化学・三菱商事によって開発されている。
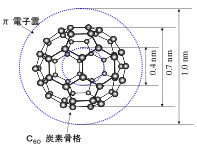
当然カーボンファミリーの混合物としてしか得られない。C60の有機溶媒への溶解性に関しては、西尾元宏著、分子間力入門、講談社サイエンティフィックに記載がある。どのような分子間力によって溶媒に溶解しているのかYMBとYSBを使って検討しよう。
化合物と溶解度のテーブルを表計算ソフトにペーストしてください。Smilesの構造式を使って、YMBで物性推算値を埋め込みテーブルを完成させてください。溶解度はmg/mlの値が記載されていますが、logをとったもので評価してください。
予測化合物
一般的に言って、多芳香環化合物、塩素含有芳香族化合物、含硫黄化合物で溶解度が高そうです。こうしたC60の定性的な溶解性に関してはハンセンの溶解度パラメータ(HSP)を使ったものがこのPirika HPにあるので参照してください。
ここではYMBを使って、より定量的に溶解性を扱かってみましょう。YMBの作り出す物性値から変数を4つ選択させてモデル式を作成してください。(変数選択は自動で、細かい刈り込みは行わないでやってみてください。)
YMBを使って推算値を得る方法はこちらを参照してください。
変数選択のやり方はこちらを参照してください。
log(C60溶解度)=0.2843*log(Henry)+0.1589*Hildebrand SP-0.1963*Hansen dH+14.1627*Refractive Index-22.8135赤四角はモデルを作るのに使わなかった予測データ用の化合物で、このモデルで良好に予測できていることがわかります。
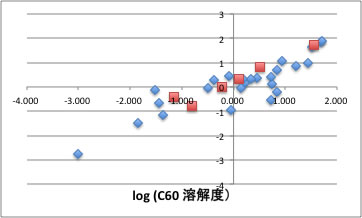
対応するブラウザーを使い、上のキャンバスに分子を描けばどのくらいの溶解度かを得る事ができます。
このように、一旦モデル式が作成できれば容易に新しい溶媒を使った時の溶解度を推算できます。
それをバッチで走らせて一番いいものを探すなども簡単にできてしままいます。
色々な溶媒の溶解度を計算してみてください。
社会に出てからも、こうしたサイクルをまわせば他所(先輩)に負けない研究ができるようになるでしょう。
しかし、コンピュータだけに頼らず”何故”を考えるのは非常に重要です。
一番大きく効いているのは屈折率です。
下の図に示すように、屈折率の大きい溶媒ほど溶解度が高いことが見て取れます。
(屈折率推算の詳しい説明はPirikaのこちらを参照してください。)
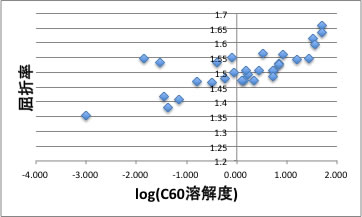
何故、屈折率の高い溶媒ほどフラーレンの溶解性が高いのでしょうか?
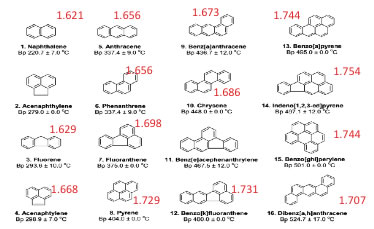
ポリ・アロマティクスの屈折率を推算すると以下のようになります。
芳香環が多くなるにつれ屈折率は高くなります。
従って似たものは似たものを溶かすの原理で溶解度が上がっていくと考えられています。
硫黄とか塩素原子は屈折率をあげることが知られています。
(ポリアロマティクスのハンセン溶解度パラメータ、HPLCの結果はPirikaのこちらの記事で説明しています)
ハンセンの溶解度パラメータのうち分散項(dD)は下図に示すように屈折率と相関があることが知られています。
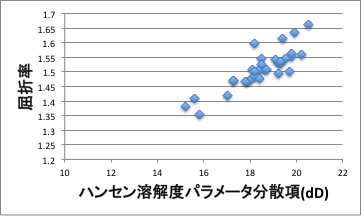
従って、C60は主にファンデルワールスの力によって溶解していることが示唆されます。

また、大まかには分子体積とも相関があり、分子が大きいほど溶解度も大きくなります。
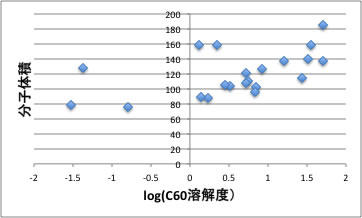
この2つの効果が溶解度を決める主要因です。
log(C60溶解度)とハンセンのdD, 分子体積の重回帰式を構築し、予測化合物セットとともにグラフを作製してください。
フラーレンを分散させる汎用ポリマーとしてはどんなものがいいか、コストを度外視するとして、そのポリマーを改良するにはどうすればいいか考えてみましょう。
分子間力を大まかに分類すると次のようになります。
ファンデルワールス相互作用: |
<1 KJ/mol |
分散項(δD) |
静電的相互作用: |
10-30KJ/mol | 分極項(δP) |
水素結合的な相互作用: |
10-30KJ/mol |
水素結合項(δH) |
その他: |
(δH) |
この中でC60の溶解性に効いているのが、ファンデルワールスの力(dD)とπ/πスタッキングでしょう。
(ハンセンの溶解度パラメータ(HSP)では、π/πスタッキングの分子間力は、その他の力としてδH:水素結合項に含まれる。)
課題:英国ケンブリッジ大学でインクジェット・プリンターで印刷できるグラフェンの透明インクを開発したというニュースがありました。(2011.11.28)
そこでは、Poly[5,5’-bis(3-dodecyl-2-thienyl)-2,2’-bithiophene] PQT-12 をバインダーポリマーとして用いています。
このポリマーの屈折率、dDをYMBを用いて計算してみましょう。
参照としてポリベンズイミダゾール(PBI)、などのポリマーの屈折率、dDも計算してみましょう。
これらのポリマーはカーボンナノチューブ(CNT)用のバインダー・ポリマーとしてPirikaが提案しています。
グラフェンのπーπスタッキングに関しては太陽電池の講義資料を参照
イオン液体ゲルも参照してください CNTをディスプレーに使った東レの例は表示素材の資料を参照のこと
東レ、東邦テナックス、三菱レイヨンで世界の70%シェアーを持っています。
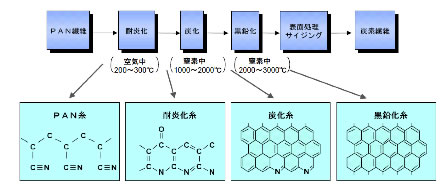
(財)航空機国際共同開発促進基金の記事から
こうした炭素繊維は、ゴルフクラブのシャフト、釣り竿、最近ではB−787の機体に採用されるなど利用範囲が非常に広がっています。実際の利用形態としては、この炭素繊維をエポキシ樹脂で固めたFRPの形で用います。軽量化で、省エネルギーに寄与することが航空機で実証された事によって、自動車などに爆発的に利用される可能性が高くなっています。
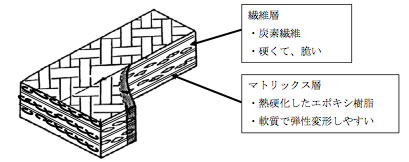
機械システム振興協会資料より
課題:
炭素繊維はどのようなエポキシ樹脂と相性がいいのでしょうか?
フラーレンの場合、ファンデルワールス力の大きい、屈折率の大きな溶媒との相互作用が大きく溶解度が高くなりました。
以下のエポキシ樹脂のうち、どれが炭素繊維と一番よく相互作用しバインダーとしての性能が高くなると思いますか?
YMBを使い基本骨格を計算し理由を述べてください。
また特許を検索しB787にはどのエポキシが使われているか確認しましょう。
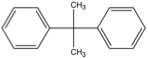 |
ビスフェノールA |
屈折率 |
ビスフェノールF |
屈折率 dD |
|
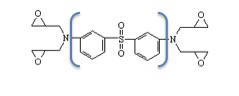 |
小西 | 屈折率 dD |
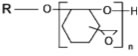 |
ダイセル | 屈折率 dD |
さらに接着性をあげるには、どうしたらいいか考えて分子設計してみましょう。
(ヒント:芳香族に直結した塩素)
三洋電機:黒鉛炭素質を負極材料
日立化成:塊状人造黒鉛負極材、世界トップシェア40%
昭和電工:人造黒鉛電極。電気炉製鋼法で鉄を溶解するのに使う黒鉛棒(陰極)がはじまり。カーボンナノチューブ(CNT)で充放電安定性
JFEケミカル:JFEは新日鉄についで日本2位、世界5位の高炉メーカー。鉄は鉄鉱石と石炭から作る。煤を作るのはお手の物。
この負極用のバインダー樹脂については、PirikaのHP、ポリビニリデンフルオライドのページを参照してください。
活性炭はヤシ殻などを蒸し焼きにして作るため原料によって吸着性能が異なりますが、一般的な吸着性能は大きくは変わりません。
課題:
次のHPから活性炭の吸着量のデータをダウンロードして吸着物質の一覧表を作りました。Smilesの構造式を使って、物性の推算値をまとめましょう。
活性炭の吸着量
吸着量と沸点をプロットすると相関があるため、沸点が高いほど吸着量は大きくなるという説がまかり通っています。
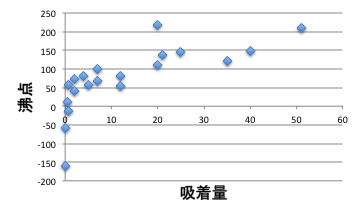
しかし、同じぐらいの沸点を持つ化合物で比べてみると、極性基を持つほど活性炭への吸着量は減るので、この考え方には矛盾があります。
|
吸着量 |
BP |
BENZENE |
12 |
80 |
METHYL ETHYLKETONE |
4 |
80 |
Acrylonitrile |
2 |
74 |
変数選択の重回帰計算を行なって、吸着量の予測式を作りましょう。 変数を3つ選んで作ったモデルは次のようになりました。
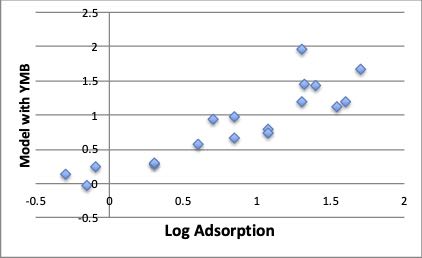
課題:
活性炭の吸着量を予測する推算式を作ってみましょう。
対応するブラウザーを使い、上のキャンバスに分子を描けばどのくらいの吸着量かを得る事ができます。 詳しい分子の描き方はこちらを参照してください。
このように、一旦モデル式が作成できれば容易に未知の化合物の吸着量を推算できるようになります。 吸着は単層吸着だけではないので複雑ですが、BETの吸着面積を考えたときに吸着できる分子の数は分子のサイズによって異なるでしょう。
当然のことながら、一般的には沸点が高くなると、分子も大きくなり、分子の表面積が増えます。本来吸着量と比べなくてはならないのはこの分子表面積であると考えられます。
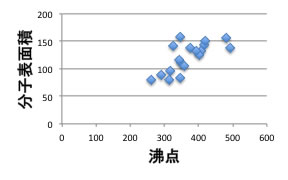
ハンセンのSP値を3次元に分割してプロットしてみると、以下のようになります。
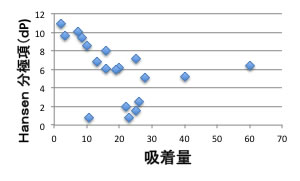
分極項(dP)は小さいほど吸着量は多くなることがわかります。
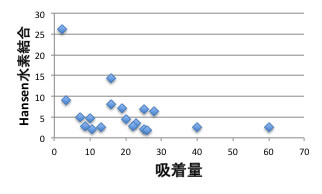
また、水素結合項(dH)も小さくなるほど吸着量は多くなることがわかります。
すなわち、非極性で分子表面積が大きいものほど多く吸着することになります。
従って活性炭の吸着の場合もフラーレンの溶解性と同様に分散項(dD)だけが大きく(ファンデルワールスの力)分子が大きいものがたくさん吸着されることがわかります。
ちなみに、鉛筆で紙に書いた文字が消しゴムで消すことができるのは、グラファイト(黒鉛)がファンデルワールスの力だけでセルロースに載っているだけなので、消しゴム(塩化ビニルにフタル酸系可塑剤を入れ固めたもの)のより大きなファンデルワールスの力でそちらに溶解してしまうためと説明されます。
また、こうした炭素材料はπ/πスタッキング:芳香環同士の相互作用を持つため、小さいながらdHを持っています。また平面から外れるカーボン・ナノチューブ(CNT)やフラーレンでは分極項(dP)も発生していると考えた方が良さそうです。日本のお家芸の炭素材料の改良に貢献するには、こうした分子間力を正しく理解する必要があると思うのですがどうでしょうか?
太陽電池の資料ではこのエネルギーを化学工学的に評価する方法を提案しています。参考にしてください。
Copyright pirika.com since 1999-
Mail: yamahiroXpirika.com (Xを@に置き換えてください) メールの件名は[pirika]で始めてください。